Что такое сперма (семенная жидкость, эякулят)?
Сперма (семенная жидкость, эякулят) была открыта в 1677 году голландским микроскопистом Антони ван Левенгуком. Представляет собой жидкость светло-серого мутного цвета, вязкую и опалесцирующую.
Как образуется сперма?
Ее первичное образование происходит в период полового созревания. Подробнее о процессе образования спермы читайте здесьОбъём эякулята
Примерный объем спермы, выделяемой при эякуляции, составит одну чайную ложку — 3 грамма. Хотя на практике могут быть варианты от 2 до 6 граммов. Ежедневно при воздержании количество спермы увеличивается на 0,4 грамма. У здорового мужчины при одной эякуляции, происходит выброс около 80 миллионов сперматозоидов, причем 3% от них — эякулят, остальные 97% представляют собой секрет предстательной железы в сочетании с жидкостью семенных пузырьков. Первая порция эякулята характеризуется высоким содержанием сперматозоидов, последующие имеют их намного меньше.
Типы и строение сперматозоидов
Мужские половые клетки или сперматозоиды передают генетическую информацию отца своему потомству. По форме напоминают головастиков и способны двигаться не только по организму, но и извне за счет своего «хвоста». Сам хвост движется змееподобно, изгибаясь в нескольких местах одновременно. Подсчитано, что его нижняя часть движется 800 раз из стороны в сторону, продвигая его на 1 см вперед к яйцеклетке. В состав сперматозоидов входят 23 хромосома и одна половая.Выделяют два типа. Первый — содержащий хромосому X, другой — Y. При слиянии с яйцеклеткой сперматозоид Х проводит к рождению девочки, Y — мальчика. Во время семяизвержения в яйцеклетку может проникнуть всего один сперматозоид.
Цикл жизни сперматозоидов
Составляет всего 72 дня, проведенных в яичках, и 12 дней существует в придатках. Полный уровень зрелости достигается в общей сложности примерно за три месяца. Активны в течение месяца, после погибают. При разложении образуют питательные вещества, в том числе белки.
состав, цвет, функции и нормальное количество
Семенная жидкость, или плазма, является тем веществом, которое вырабатывается семенными пузырьками и секретом предстательной железы. Вместе со сперматозоидами данный секрет превращается в сперму.
Производство и основная функция семенной жидкости
Главной функцией семенной жидкости является создание питательной среды для защиты миллионов сперматозоидов, которые в конечном счете должны достичь своей главной цели – выжить во влагалище и добраться до яйцеклетки. В итоге можно сказать, что семенная жидкость является секретом-носителем самой спермы, который вырабатывается по мере ее прохождения через семявыводящий проток от яичек к члену. После смешивания оба вещества образовывают эякуляторную жидкость, которая и выбрасывается через отверстие в половом члене.
Чтобы обезопасить и защитить сперматозоиды от кислотной среды уретры, непосредственно перед эякуляцией выделяется дополнительное количество секрета, производимого Куперовой железой. Все дело в том, что у мужчины выделение спермы и мочеиспускание производится через один канал, и, чтобы обезопасить сперматозоиды от верной гибели, вырабатывается небольшое количество нейтрализующего секрета.
Все дело в том, что у мужчины выделение спермы и мочеиспускание производится через один канал, и, чтобы обезопасить сперматозоиды от верной гибели, вырабатывается небольшое количество нейтрализующего секрета.
Состав семенной жидкости
Спермоплазма, являющаяся частью самой спермы, отличается уникальностью состава. В нее входит огромное количество специфических химических соединений, встречающихся в гораздо меньшем объеме и в других тканях человеческого организма. Комплексный состав семенной жидкости представляет собой набор белков, углеводов, жиров и ферментов, а также гормонов и других не менее обходимых веществ.
Если же рассматривать спермоплазму более подробно, то главным ее компонентом является, конечно же, вода. Также обязательно наличие простых полисахаридов, которые снабжают сперматозоиды энергией во время их длительного пути к яйцеклетке, и щелочи, нейтрализующей кислотность влагалища и уретры. Ещё семенная жидкость состоит из гормоноподобных веществ, которые приводят к сокращению фаллопиевых труб и матки и помогают сперматозоидам быстрее достичь своей цели. В качестве обязательного дополнения в составе семенной плазмы находится холестерин, цинк, и витамин С.
В качестве обязательного дополнения в составе семенной плазмы находится холестерин, цинк, и витамин С.
Цвет спермоплазмы
Цвет семенной жидкости в норме может варьироваться от молочно-белого до насыщенно-кремового. Простыми словами, сперма здорового мужчины должны быть жемчужной, но иногда ее оттенки не совпадают с требуемыми нормами. К примеру, вне зависимости от интенсивности половой жизни сперма может оказаться прозрачной, что часто является первым признаком мужского бесплодия. Если же спермоплазма порозовела, значит, в ее составе появилась примесь крови, что может оказаться признаком воспаления уретры или же простаты. При любом инфекционном заболевании мошонки или семенных пузырьков сперма может оказаться грязно-желтой или даже зеленоватой. Особое внимание требует к себе бурая сперма, которая обычно становится такой от примеси старой крови. Чаще всего такой цвет «мужской» жидкости может свидетельствовать о развитии очень серьезных патологий и заболеваний.
В любом случае, если цвет выделяемой из пениса жидкости далек от жемчужного, стоит сразу же обратиться к советующему специалисту за консультацией.
Нормальное количество эякуляторной жидкости
У здорового мужчины в среднем во время эякуляции должно вырабатываться от 3 до 5 мл семенной плазмы. При этом если на протяжении некоторого периода семяизвержение не происходило, то после подобного «застоя» семенная жидкость должна вырабатываться в ускоренном количестве. Также на увеличение объема «мужского сока» может повлиять длительная прелюдия, стимулирующая готовность организма на протяжении некоторого времени. Кстати, несмотря на то что в составе семенной жидкости есть сахар, сам эякулят нельзя назвать калорийным. Каждая порция спермы, вырабатываемой при оргазме, содержит не более 25 калорий.
Нарушения выработки спермы
В некоторых случая сперма мужчины может вырабатываться в меньшем количества или же исчезнуть вовсе. К такому нарушению приводит целый ряд факторов, о которых стоит поговорить подробнее. Полное отсутствие семенной жидкости может быть вызвано увеличением массы тела, гормональными сбоями в организме, повышением температуры и венерическими заболеваниями. Такой исход является очень серьезным признаком неправильной работы мужской репродуктивной системы, поэтому лучше как можно быстрее обсудить этот симптом со своим лечащим врачом.
Такой исход является очень серьезным признаком неправильной работы мужской репродуктивной системы, поэтому лучше как можно быстрее обсудить этот симптом со своим лечащим врачом.
В итоге, чтобы чувствовать себя полноценным мужчиной во всех смыслах этого слова, важно следить за любыми изменениями в организме. Семенная жидкость будет всегда в норме, если на первом месте будет стоять правильный образ жизни, контрацепция и своевременная проверка у сопутствующего специалиста.
Семенная жидкость ослепила пчелиных цариц
Max Pixel
 Оказалось, что под действием семенной жидкости царицы начинают хуже реагировать на свет и, как следствие, с трудом попадают домой в улей. Исследователи полагают, что так проявляется конфликт полов — самцы пытаются помешать царицам спариться с другими трутнями. Работа опубликована в журнале eLife
Оказалось, что под действием семенной жидкости царицы начинают хуже реагировать на свет и, как следствие, с трудом попадают домой в улей. Исследователи полагают, что так проявляется конфликт полов — самцы пытаются помешать царицам спариться с другими трутнями. Работа опубликована в журнале eLifeХоанито Либерти (Joanito Liberti) из Копенгагенского университета и его коллеги из Австралии, Дании и США изучили, как именно спаривание влияет на экспрессию генов.
Чтобы проверить, действительно ли зрение цариц ухудшается после спаривания, исследователи провели электроретинограмму, то есть измерили активность нейронов сетчатки. На второй день после введения спермы или семенной жидкости амплитуда нервных импульсов в ответ на световой сигнал упала — пчелы частично ослепли.
На второй день после введения спермы или семенной жидкости амплитуда нервных импульсов в ответ на световой сигнал упала — пчелы частично ослепли.
Затем ученые снабдили цариц радиомаячками и выпустили их из улья, чтобы посмотреть, как спаривание влияет на их дальнейшее передвижение. У входа в улей установили датчики, реагирующие на прикосновение. Среди самок, которые получили инъекцию физраствора, обратно в улей вернулись практически все. Те же, кому ввели сперму или семенную жидкость, гораздо чаще терялись — около половины из них заблудились и не смогли попасть домой. Кроме того, они чаще задевали датчики на входе в улей: внутри гораздо темнее, чем снаружи, и пчелам было непросто найти отверстие и попасть в него.
Феномену ослепления пчелиных цариц после спаривания можно придумать несколько объяснений. Например, авторы работы предположили, что зрение может падать в целях экономии ресурсов: нервная система потребляет много энергии, но самке после спаривания нужно бросить все ресурсы на размножение.
Исследователи придерживаются другой версии развития событий — они считают, что здесь разворачивается конфликт полов. Самки пытаются максимально разнообразить свое потомство, а самцы заинтересованы в обратном. И поскольку царицы вылетают на спаривание несколько дней подряд, то семенная жидкость не лишает их репродуктивного успеха в первый же день, но в последующие сильно затрудняет передвижение и мешает разглядеть не только потенциальных половых партнеров, но и собственный улей.
Но иногда влияние семенной жидкости на организм царицы бывает и благотворным — например, в ней могут содержаться противогрибковые вещества.
Полина Лосева
Семенная жидкость улучшила память самок дрозофил
Ученые выяснили, что самцы мух влияют на поведение самок после спаривания, а именно улучшают их долговременную память.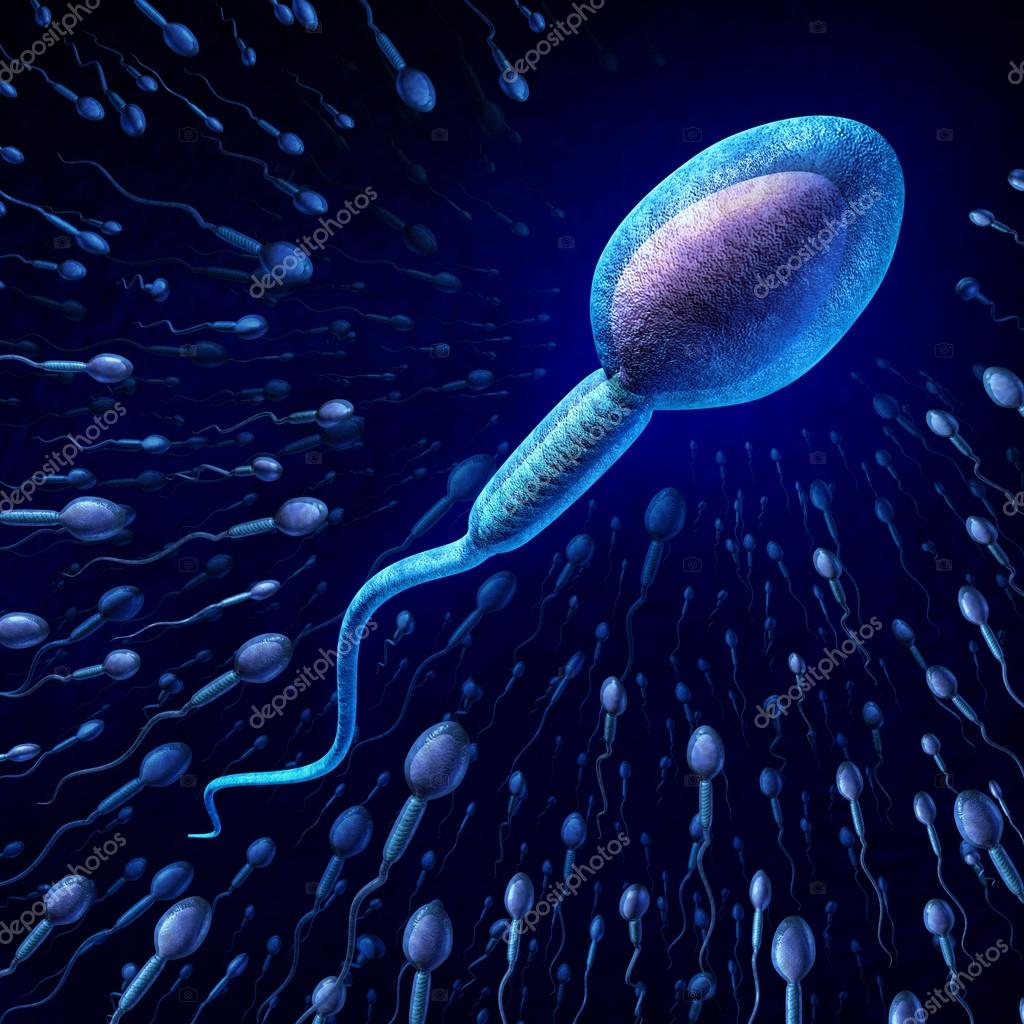 В этом замешан белок из их семенной жидкости, которые действует напрямую на нейроны самки, усиливая их активность. Исследование опубликовано в журнале
В этом замешан белок из их семенной жидкости, которые действует напрямую на нейроны самки, усиливая их активность. Исследование опубликовано в журнале
Спаривание влияет на физиологию самки с разных сторон: например, снижает готовность спариваться дальше или изменяет пищевые предпочтения. На поведении и когнитивных способностях оно тоже, конечно же, сказывается, однако до сих пор до конца не ясно, как именно.
С одной стороны, есть распространенное мнение о том, что самки разных видов после оплодотворения глупеют, поскольку энергетические ресурсы от мозга перенаправляются к плоду. С другой стороны, было бы логично предположить, что при беременности страдают не все функции мозга, а некоторые оказываются полезными для будущей матери и, наоборот, укрепляются. В числе таких функций может быть, например, ориентирование в пространстве, избегание риска и способность запоминать, где находятся источники воды и еды.
Группа ученых из парижского Института наук и гуманитарных исследований под руководством Томаса Преа (Thomas Preat) проверила влияние спаривания на память у дрозофил. Ранее исследователи уже обнаруживали, что влияние спермы на организм мух опосредованно SP — семенным белком. Рецепторы к ней обнаружены в матке и нервной системе дрозофил, но их функции — особенно в нервной системе — пока неясны.
Ранее исследователи уже обнаруживали, что влияние спермы на организм мух опосредованно SP — семенным белком. Рецепторы к ней обнаружены в матке и нервной системе дрозофил, но их функции — особенно в нервной системе — пока неясны.
Ученые проводили на мухах стандартный эксперимент по выработке избегающего поведения: им предлагали определенный запах, который сопровождали ударом тока. Затем мухам предлагали выбрать между ветвями лабиринта, одна из которых содержала запах-стимул, а другая не пахла ничем.
После спаривания мухи в два раза лучше справлялись с этой задачей, чем мухи, которые не спаривались с самцами. А вот те, кого скрестили с самцами-мутантами, сперма которых была лишена SP, показали такой же результат, как и неспаривавшиеся самки. Затем исследователи попробовали заменить спаривание на инъекцию SP. Самки, которые не контактировали с самцами, но получили инъекцию, проходили лабиринт так же хорошо (p = 0,004), как и самки после спаривания.
Чтобы проверить, как именно белок SP действует на память, исследователи заблокировали работу рецептора к SP в нейронах стенки матки.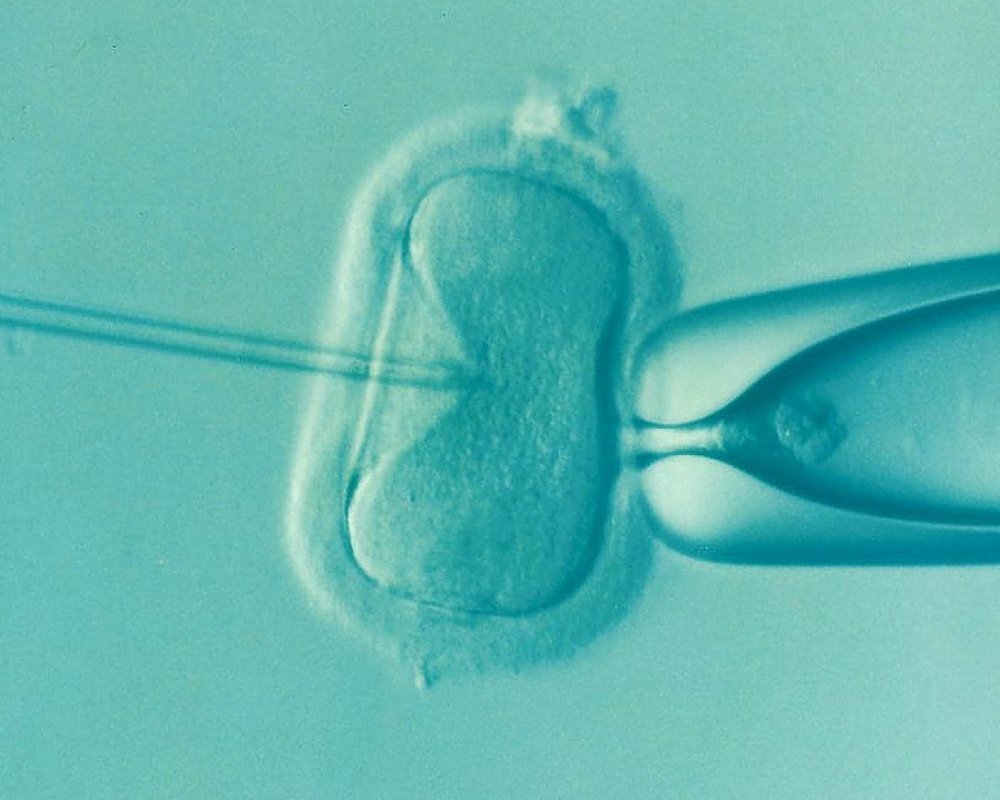 Но ничего не изменилось: мухи все так же успешно (p = 0,009) проходили лабиринт после спаривания. Тогда ученые предположили, что SP может влиять на работу серотонинергических нейронов — известно, что их активность связана с памятью у мух. И действительно, рецепторы к SP удалось обнаружить на нейронах в брюшной нервной цепочке и мозге дрозофил.
Но ничего не изменилось: мухи все так же успешно (p = 0,009) проходили лабиринт после спаривания. Тогда ученые предположили, что SP может влиять на работу серотонинергических нейронов — известно, что их активность связана с памятью у мух. И действительно, рецепторы к SP удалось обнаружить на нейронах в брюшной нервной цепочке и мозге дрозофил.
Работу серотонинергических нейронов у мух регулирует фермент фосфодиэстераза. Ученые измерили ее активность и выяснили, что после спаривания она в два раза ниже, чем у не спаривавшихся мух, — то есть позволяет нейронам быть более активными. Когда же ее работу заблокировали, мухи, не контактировавшие с самцами, стали проходить лабиринт так же хорошо (p = 0,003), как и самки после спаривания.
Авторы работы полагают, что хорошая память на запахи может иметь важное адаптивное значение для беременных мух — например, она позволяет им аккуратнее выбрать место для кладки, чтобы рядом не было врага или какого-нибудь ядовитого вещества.
Ранее ученые уже обнаруживали необычные свойства у спермы разных организмов. Например, человеческая семенная жидкость подавляет воспаление в женских половых путях и облегчает наступление беременности. Пчелиная сперма ослепляет цариц, чтобы они не покидали улей и не спаривались с другими самцами. А возраст спермы у рыбок данио-рерио определяет здоровье и долголетие потомства.
Например, человеческая семенная жидкость подавляет воспаление в женских половых путях и облегчает наступление беременности. Пчелиная сперма ослепляет цариц, чтобы они не покидали улей и не спаривались с другими самцами. А возраст спермы у рыбок данио-рерио определяет здоровье и долголетие потомства.
Полина Лосева
Нарушения сперматогенеза — справочник болезней — ЗдоровьеИнфо
После изучения анамнеза и проведения общего обследования врач назначает анализ семенной жидкости – основной метод, применяемый для диагностики мужского бесплодия. Мужчине рекомендуется избегать половых контактов и эякуляции в течение 2-3 дней перед исследованием. Для его проведения необходимо вызвать эякуляцию, обычно путем мастурбации, в чистую стеклянную пробирку предпочтительно непосредственно в лаборатории. У мужчин, имеющих трудности с получением образца семенной жидкости этим путем, могут использоваться специальные презервативы, которые не имеют никаких смазок или веществ, токсичных для спермы, чтобы собрать семенную жидкость во время полового сношения. Более надежно исследование, которое выполнено на основании двух или трех образцов спермы, полученных отдельно.
Более надежно исследование, которое выполнено на основании двух или трех образцов спермы, полученных отдельно.Если в семенной жидкости обнаруживают патологические изменения, то анализ обычно повторяется, поскольку образцы, взятые от одного и того же мужчины, в норме очень изменчивы. Если семенная жидкость все же имеет патологию, врач устанавливает ее возможные причины. Это могут быть последствия перенесенного паратифа с осложнением на яички (орхит), острое заболевание или длительное повышение температуры тела в течение предыдущих 3 месяцев, травма яичек, воздействие промышленных токсинов или вредных факторов окружающей среды, использование диэтилстилбэстрола или анаболических стероидов, использование наркотиков и злоупотребление спиртным. Малое число сперматозоидов может, однако, указывать лишь на то, что после последней эякуляции прошло недостаточно времени или, что была собрана только часть семенной жидкости.
Врач обследует мужчину для выявления возможных заболеваний, например крипторхизма (неопущения яичка), а также признаков наследственных или гормональных заболеваний, которые могли бы объяснять бесплодие. Гормональные нарушения, при которых уменьшается выработка тестостерона (гипогонадизм), обусловлены заболеваниями яичек или других желез, например гипофиза.
Гормональные нарушения, при которых уменьшается выработка тестостерона (гипогонадизм), обусловлены заболеваниями яичек или других желез, например гипофиза.
Прежде чем использовать методы искусственного оплодотворения, в центрах репродукции проводят исследование сперматогенеза и качества спермы. Один из таких анализов позволяет обнаруживать антитела к сперматозоидам; другой – определять, не повреждены ли их оболочки. Специальные методы исследования дают возможность оценить подвижность сперматозоидов и их способность проникать в яйцеклетку.
Как устроена мужская репродуктивная система
КАКИЕ ГОРМОНЫ РЕГУЛИРУЮТ РАБОТУ МУЖСКОЙ
РЕПРОДУКТИВНОЙ СИСТЕМЫ?
Работа мужской репродуктивной системы главным образом зависит от трех гормонов. Лютеинизирующий (ЛГ) и фолликулостимулирующий (ФСГ) гормоны вырабатываются гипофизом — железой, которая находится у основания головного мозга. ФСГ стимулирует образование сперматозоидов, ЛГ — синтез тестостерона.
Тестостерон необходим для производства спермы, а также возникновения вторичных половых признаков: увеличения мышечной массы, роста волос на теле по мужскому типу, полового влечения к женщинам, низкого голоса и др.
КАК ОБРАЗУЕТСЯ СПЕРМА?
Производство спермы называется сперматогенезом. Он может происходить только под влиянием гормонов, поэтому до полового созревания (12–16 лет) организм мальчика не способен производить сперматозоиды.
Когда в организме подростка повышается уровень тестостерона, активируется сперматогоний — особые стволовые клетки в яичках. Они превращаются в сперматоциты. Эти клетки содержат двойной набор хромосом, после деления из них образуются вторичные сперматоциты, содержащие по одному набору хромосом.
У человека есть две половые хромосомы – X и Y. Яйцеклетка может содержать только хромосому X. Сперматозоид – либо X, либо Y. Если яйцеклетку оплодотворяет сперматозоид с Y-хромосомой, получается мальчик, если с X – девочка.
Из сперматоцитов образуются сперматидные клетки. На этом сложный процесс образования спермы не заканчивается. Сперматидные клетки проходят через процесс, известный как спермиогенез. У них отрастают хвостики, и они приобретают черты, характерные для сперматозоидов. После дозревания в придатке яичка они готовы покинуть организм мужчины в поисках яйцеклетки.
После дозревания в придатке яичка они готовы покинуть организм мужчины в поисках яйцеклетки.
Зрелый сперматозоид умеет передвигаться со скоростью 20 см в час. И это при том, что его длина составляет 0,05 мм.
БЫВАЕТ ЛИ У МУЖЧИН МЕНОПАУЗА?
Термин «менопауза» обозначает прекращение менструаций у женщин. Происходит это из-за падения уровня половых гормонов. В норме в мужском организме такого происходить не должно. Яички могут вырабатывать сперму и в 80 лет, и в более старшем возрасте.
Однако у некоторых мужчин уже в 40–50 лет уровень тестостерона снижается, производство спермы падает. Нередко это происходит на фоне хронических заболеваний, таких как сахарный диабет. Считается, что это может приводить к таким симптомам, как эректильная дисфункция (ослабление эрекции), депрессия, слабость. Иногда такое состояние называют «мужской менопаузой». При низком уровне тестостерона назначают гормональную заместительную терапию.
Доктора Института репродуктивной медицины REMEDI знают всё о репродуктивном мужском здоровье. Мы знаем, как его сохранить и восстановить, подарить мужчине способность иметь детей.
Семенная жидкость: функции, воспроизводство и состав » MyMensClub.ru
Семенная жидкость и сперма — не одно и тоже. Многие из нас, думая о ней, подразумевают сперму, но семенная жидкость является лишь частью ее. Сперматозоиды составляет менее 10 процентов мужской спермы, остальное — это семенная жидкость. В среднем при каждой эякуляции выбрасывается от 120 до 600 миллионов сперматозоидов, чего теоретически почти достаточно для того, чтобы еще раз заселить мир. В остальных 90 с лишним процентах мужского эякулята содержится свыше 30 различных веществ.Главная функция семенной жидкости — обеспечить защиту и питательную среду для тех сотен миллионов сперматозоидов, которые должны выжить во влагалищной среде и достичь конечной цели — яйцеклетки. Этот секрет-носитель спермы изначально производится 3 железами, находящимися внутри тела — семенными пузырьками, предстательной железой и куперовыми железами. По мере того как сперма проходит вверх от яичек к члену через семявыносящий проток, предстательная железа и семенные пузырьки вырабатывают жидкости, которые затем смешиваются со спермой, после чего полученная эякуляторная жидкость проходит через половой член и выбрасывается из него. Непосредственно перед эякуляцией выделяется еще несколько капель секрета (предэякулята), вырабатываемого Куперовой железой (она находится в корне члена), который служит для нейтрализации кислотной среды уретры и защиты сперматозоидов от причинения им вреда или гибели.
Поскольку у мужчин мочеиспускание происходят через тот же канал, что и семяизвержение, эта система создана для того, чтобы защитить сперматозоиды и обеспечить продолжение человеческого рода. Без добавления этого нейтрализующего секрета и составных компонентов семенной жидкости у Адама и Евы могло бы никогда не быть потомков.
Итак, что же это за защитные и энергоснабжающие жидкости, какой состав семенной жидкости? Основные ингредиенты следующие:
вода;
простые сахара для снабжения сперматозоидов энергией;
щелочи для нейтрализации кислотности уретры и влагалища;
простагландины-гормоноподобные вещества, присутствующие в различных тканяхи жидкостях человеческого тела (включая матку, почки, легкие и головной мозг), которые вызывают сокращения матки и фаялопиевых труб, помогая сперматозоидам достичь яйцеклетки;
витамин С;
холестерин;
цинк.
Характерный цвет семенной жидкости обычно жемчужный — от молочно-белого до кремового. Она может быть более желтой, если у мужчины какое-то время не было эякуляций. Оттенок от розового до коричневого может указывать на наличие крови. Это не причина для немедленной тревоги, однако если кровь постоянно присутствует в эякуляте, обратитесь к своему участковому терапевту, поскольку это может быть признаком инфекции или рака простаты.
Среднее количество семенной жидкости, выбрасываемой при эякуляции, составляет от 3 до 5 мл (примерно чайная ложка), но ее количество может возрастать, если мужчина какой-то период не эякулировал, или уменьшаться если у него было несколько эякуляций подряд. В любом случае, на следующий день объем эякулята обычно возвращается в норму. Продолжительная прелюдия также может увеличить количество выбрасываемой семенной жидкости при эякуляции, поскольку при долгой сексуальной стимуляции готовность организма достигается в течение большего времени, в связи с чем такие органы, как предстательная железа, вырабатывают больше жидкости. Несмотря на то что семенная жидкость содержит сахара, эякулят не является калорийным. Каждая порция жидкости, выбрасываемая при эякуляции, содержит от 5 до 25 калорий, поэтому, девушки, ее глотание не испортит вашу фигуру))))))
Что ваша сперма говорит о вашем здоровье
Сперма — это мутная белая телесная жидкость, которая выделяется из уретры и полового члена во время эякуляции. Он состоит из подвижных сперматозоидов (называемых сперматозоидами) и богатой питательными веществами жидкости, называемой семенной жидкостью. Семенная жидкость предназначена как для транспортировки сперматозоидов, так и для повышения их способности к оплодотворению.
Вот несколько ответов на распространенные вопросы о сперме.
Как производится сперма?
Сперматозоиды вырабатываются в яичках, хранятся в придатках яичка и составляют менее 10% спермы — лакомый кусок, который может вас удивить.Во время эякуляции толстостенный проток, называемый семявыносящим протоком, переносит сперматозоиды из придатка яичка в уретру, а затем за пределы тела или во влагалище посредством полового члена.
Когда сперматозоиды проходят через семявыносящий проток, три разные железы выделяют слизистые выделения (называемые семенной жидкостью), которые объединяются со сперматозоидами для образования спермы. Эти три железы, которые часто называют дополнительными половыми железами, — это бульбоуретральные железы (также называемые железами Купера), предстательная железа и семенные пузырьки.
Веривелл / JR BeeКаперовы железы
Первая порция семенной жидкости (около 5%) состоит из секрета куперовских желез. Эти железы размером с горошину производят то, что называется предэякуляционной жидкостью, то есть небольшое количество жидкости, которое выделяется перед эякуляцией. Эта жидкость смазывает уретру и нейтрализует кислотность, позволяя сперматозоидам легко перемещаться.
Простата
Приблизительно от 15% до 30% спермы вырабатывается предстательной железой, железой размером с грецкий орех, расположенной у основания мочевого пузыря, окружающего уретру мужчины.Предстательная железа является основным источником кислой фосфатазы, лимонной кислоты, инозита, кальция, цинка и магния.
Все эти уникальные компоненты играют роль. Например, цинк считается антибактериальным фактором. Интересно, что некоторые эксперты считают, что это может быть одной из причин, по которой инфекции мочевыводящих путей не так распространены у мужчин по сравнению с женщинами.
Предстательная железа также выделяет ферменты, которые разжижают сперму примерно через 15-30 минут после эякуляции.Этот процесс разжижения позволяет сперматозоидам медленно высвобождаться.
Затем сперматозоиды могут входить в шейку матки и упорядоченно перемещаться вверх по женской репродуктивной системе с конечной целью найти яйцеклетку для оплодотворения.
Семенные пузырьки (семенные железы)
Примерно от 65% до 75% семенной жидкости производится семенными пузырьками, которые расположены над предстательной железой у основания мочевого пузыря и содержат такие компоненты, как фруктоза (сахар) и простагландины.
Фруктоза питает сперматозоиды, обеспечивая их энергией. Простагландины помогают вызвать сокращение мышц влагалища, чтобы продвинуть сперму вверх по влагалищному каналу и через шейку матки.
Факторы свертывания также присутствуют в жидкости, секретируемой семенными пузырьками. Это заставляет сперму слипаться, образуя желеобразную консистенцию сразу после эякуляции.
Цель процесса свертывания крови — удерживать сперму на месте до тех пор, пока она не сможет медленно высвобождаться во время процесса разжижения (контролируемого ферментами, секретируемыми предстательной железой).
Каков запах и вкус спермы?
Сперма часто имеет запах хлора и слегка сладковатый вкус из-за высокого содержания фруктозы. При этом вкус спермы имеет тенденцию незначительно меняться от человека к человеку.
Если ваша сперма имеет неприятный запах, обратитесь к врачу, поскольку это часто является признаком инфекции.
Какой объем эякуляции?
Объем спермы, выделяемой во время эякуляции, варьируется в зависимости от исследований, хотя обзорное исследование в журнале Journal of Andrology предполагает, что средний объем составляет около 3.4 мл. Кроме того, два фактора, которые могут повлиять на объем спермы во время эякуляции, включают время последней эякуляции и состояние гидратации.
На что указывает цвет спермы?
Нормальная сперма может иметь беловатый или слегка желтоватый оттенок.
Красная или коричневая сперма
Если ваша сперма имеет красный или коричневый цвет, это может быть признаком крови. Хотя это может показаться вам тревожным, в большинстве случаев кровь в вашей сперме (так называемая гематоспермия) обычно доброкачественная.
Наиболее частой причиной этого является биопсия простаты, но это также может быть связано с множеством других состояний, которые влияют на органы мужского репродуктивного тракта, например, инфекция. В редких случаях кровь в сперме является признаком рака.
Хорошая новость заключается в том, что гематоспермия обычно проходит сама по себе. Тем не менее, важно, чтобы ваш врач проверил это. Скорее всего, он задаст вам вопросы, проведет обследование (особенно мошонки и предстательной железы) и проведет обследование.
Желтое или зеленое семя
Сперма с ярко выраженным желтым или зеленым цветом может указывать на инфекцию, такую как гонорея, передающаяся половым путем (ИППП).Если ваша сперма обесцвечивается из-за инфекции гонореи (она также может иметь неприятный запах), потребуется лечение антибиотиками, назначенными врачом.
Слово от Verywell
Ваша сперма не так проста, как вы могли подумать. В нем много компонентов, каждый из которых играет роль в улучшении воспроизводства — ваша сперма достигает овулированной яйцеклетки.
Однако важно отметить, что жидкая часть не является абсолютно важной для оплодотворения, о чем свидетельствует внутрицитоплазматическая инъекция сперматозоидов, при которой в яйцеклетку вводится один сперматозоид.
Конечно, если у вас есть какие-либо вопросы или опасения по поводу вашей спермы, обратитесь к своему врачу — и не смущайтесь, это то, чему они обучены.
Физиология спермы
У всех видов сперма переносит сперму в репродуктивный тракт самки для облегчения оплодотворения.
У некоторых видов оплодотворение может происходить извне. При внешнем оплодотворении сперматозоид оплодотворяет яйцеклетку непосредственно за пределами половых органов женщины.Таким образом оплодотворяются несколько рыб.
Внутреннее оплодотворение чаще встречается у млекопитающих, таких как люди. При этом оплодотворение происходит внутри женских половых органов. Мужчина должен эякулировать и депонировать сперму в женских половых путях посредством совокупления. Сперматозоиды попадают в тракт к ожидающей яйцеклетке и оплодотворяют ее.
Сперма человека
Состав
Большая часть жидкости в сперме состоит из выделений мужских репродуктивных органов.Сперма содержит лимонную кислоту, свободные аминокислоты, фруктозу, ферменты, фосфорилхолин, простагландин, калий и цинк.
- От 46 до 80 процентов жидкости вырабатывается семенными пузырьками
- от 13 до 33 процентов предстательной железой
- 5 процентов яичек и придатков яичка
- 2-5 процентов от бульбоуретральных и уретральных желез
Нормальный образец спермы
Нормальная сперма имеет определенные характеристики.Их можно разбить на внешний вид, объем, запах и т. Д.
Внешний вид человеческой спермы
Обычный образец имеет серо-опалесцирующий вид. Если оставить сперму открытой на какое-то время, в течение первого часа она сначала свертывается или коагулирует, а затем становится жидкой.
Объем
Обычный объем спермы на эякулят составляет от 2 до 3 мл или более. Сперма составляет примерно 10% от объема спермы.
Запах
Запах хлора или рыбный запах в сперме — это нормально.
Вкус
Сперма на вкус слегка сладкая из-за высокого содержания фруктозы. Вкус спермы имеет тенденцию незначительно меняться от человека к человеку и может зависеть от диеты.
pH спермы
Диапазон pH должен составлять от 7,2 до 7,8. Это нормальный pH тела. Если pH ниже 7,2, это может означать, что в репродуктивном тракте мало сперматозоидов или имеется порок развития. Если pH выше 7,8, это может указывать на инфекцию мочевыводящих путей.
Концентрация спермы
Нормальный диапазон сперматозоидов в образцах спермы составляет 20 миллионов / мл или больше, а общее количество — 40 миллионов или больше.
Подвижность и жизнеспособность
Для успешного оплодотворения сперматозоиды должны двигаться и жить. Для фертильности мужчины должны быть активными не менее 50% наблюдаемых сперматозоидов. Сперма через час после эякуляции движутся по прямой линии.
Морфология или структура сперматозоидов
После выпуска сперматозоиды созревают в семенных канальцах до зрелых сперматозоидов овальной формы и имеют акромсомальный колпачок. В сперме некоторые клетки показывают разные стадии зрелости.У некоторых есть сужающиеся головки; булавочные головки, круглые головки и т. д. Это не зрелые сперматозоиды. Образец спермы обычно содержит 50% или более нормальных сперматозоидов.
Лейкоциты в сперме
Это может указывать на инфекцию мочевыводящих или половых путей.
Фруктоза
Фруктоза — самый крупный компонент спермы. Отсутствие фруктозы в сперме означает непроходимость или отсутствие семявыносящего протока.
Развитие спермы
Сперматозоиды развиваются более 70 дней и производятся исключительно в яичках.Отдельные сперматозоиды развиваются в яичках из клетки, называемой сперматогониумом. Они делятся с образованием сперматоцитов, которые затем развиваются в сперматиды.
У сперматид есть хвост, и клетка постепенно приобретает способность двигаться, взмахивая хвостом. Сперматида со временем превращается в зрелые сперматозоиды. Этот процесс занимает около 60 дней. Еще от 10 до 14 дней необходимо, чтобы пройти через протоки каждого яичка и придатка яичка, прежде чем он сможет покинуть тело в сперме во время эякуляции.
Анализ спермы
Невозможность оплодотворения яйцеклетки приводит к бесплодию у пары. В этих случаях сперма от партнера-мужчины собирается для анализа.
Анализ спермы является наиболее важным критерием оценки мужского бесплодия. Это простой и недорогой клинический тест. Всемирная организация здравоохранения (ВОЗ) предоставляет критерии анализа спермы для выявления аномалий в сперме партнера-мужчины, способствующих бесплодию.
Нормальные качества спермы и сперматозоидов по данным Всемирной организации здравоохранения:
- Для фертильности должно быть не менее 20 миллионов сперматозоидов на миллилитр
- общий объем спермы должен быть не менее 2 мл
- в эякуляте должно присутствовать не менее 40 миллионов сперматозоидов
- По крайней мере 30 процентов сперматозоидов должны быть зрелыми и развиваться
- не менее 75 процентов сперматозоидов должны быть живыми или жизнеспособными
- По крайней мере 25 процентов сперматозоидов должны плавать с быстрым движением вперед
- По крайней мере, 50 процентов сперматозоидов должны плавать, даже если они вялые
Дополнительная литература
намного больше, чем предполагалось ранее
J Assist Reprod Genet.2014 июн; 31 (6): 627–636.
Джон Дж. Бромфилд
Департамент зоотехники, Университет Флориды, а / я 110910, Гейнсвилл, Флорида, 32611-0910 США
Департамент наук о животных, Университет Флориды, а / я 110910, Гейнсвилл, Флорида 32611-0910 США
Автор, ответственный за переписку.Поступило 6 марта 2014 г .; Принято, 2014 г. 22 апреля.
Авторские права © Springer Science + Business Media, Нью-Йорк, 2014 г.Abstract
Влияние семенной плазмы на цитокины и иммунную среду матки хорошо изучено у мышей и людей, в то время как влияние нарушения воздействия семенной плазмы матки на беременность и здоровье потомства становится все более понятным. Клеточная и молекулярная среда матки в период до и после имплантации на ранних сроках беременности имеет решающее значение для успеха имплантации и оптимального развития плода и плаценты. Нарушения в этой среде не только имеют последствия для благополучия беременности и здоровья и жизнеспособности новорожденных, но также могут привести к неблагоприятным последствиям для здоровья потомства после рождения, особенно к развитию метаболических нарушений, таких как ожирение, гипертония и инсулинорезистентность.В настоящее время сообщается, что отсутствие семенной плазмы при зачатии у мышей способствует увеличению накопления жира, изменению метаболизма и гипертонии у потомства. Приведенные здесь данные демонстрируют, что семенная плазма является не просто транспортной средой для сперматозоидов, но действует также как ключевой регулятор среды женского тракта, обеспечивая оптимальную поддержку развивающегося эмбриона и принося пользу будущему здоровью потомства.
Ключевые слова: Семенная жидкость, Программирование, Воспаление, Фертильность
Введение
Процесс осеменения больше не рассматривается просто как доставка спермы в женские половые пути [1].Хотя это может быть основной целью оплодотворения, в настоящее время есть доказательства того, что сперма может воздействовать непосредственно на ткани женского репродуктивного тракта, вызывая дополнительные функции, которые, в свою очередь, могут влиять на имплантацию, развитие предимплантационного эмбриона и будущее здоровье потомства. . За последнее десятилетие в семенной плазме были идентифицированы специфические соединения, которые могут проявлять биологическую активность в клетках женского тракта. Однако очевидно, что цельная сперма не является абсолютным требованием для жизнеспособного исхода беременности, о чем свидетельствует появление переноса эмбрионов и искусственного оплодотворения.Таким образом, оказывается, что семенные факторы действуют в первую очередь для оптимизации вероятности успешной беременности. Это подтверждается исследованиями, показывающими, что добавление семенной плазмы или семенных факторов к вспомогательным репродуктивным процедурам может заметно улучшить беременность у мышей, крыс, хомяков, овец и людей [2–6].
Исследования на мышах продемонстрировали важность цитокинов, присутствующих в семенной жидкости. В частности, было описано, что семенной трансформирующий фактор роста-бета (TGFβ) [7] взаимодействует с эпителиальными клетками матки, индуцируя экспрессию ряда провоспалительных цитокинов, что приводит к классической воспалительной реакции, кульминацией которой является приток лейкоцитов. в ткани эндометрия [8].Предполагается, что этот воспалительный ответ на сперму и связанное с ним изменение цитокиновой среды опосредует несколько последующих эффектов в женских репродуктивных трактах [9]. Совсем недавно эти исследования были повторены на людях, особенно на шейке матки после полового акта [10–12]. Недавно мы сообщили, что беременность, начавшаяся в отсутствие семенной плазмы у мышей, дает потомство с измененными метаболическими профилями, ожирением и гипертонией, частично из-за нарушений в периконтинентальной среде и экспрессии эмбриотрофных цитокинов в яйцеводах [13].
Воспалительные изменения, вызванные осеменением, могут быть связаны с иммунными изменениями, необходимыми для адаптации к беременности. Введение аллогенного материала в организм хозяина обычно сопровождается быстрым отторжением ткани иммунной системой хозяина. Выживание полуаллогенного концептуса внутри его матери — исключение из этого общего правила. Считается, что процесс выживания эмбриона посредством имплантации и беременности опосредуется подавлением материнского иммунитета или иммунным отклонением, процессом, при котором цитокиновая среда может определять качество иммунного ответа для достижения функциональной иммунной толерантности.События, приводящие к этим иммунным изменениям во время беременности, неизвестны, но предполагается, что они начинаются при оплодотворении, когда материнская иммунная система впервые подвергается воздействию отцовских трансплантируемых антигенов, некоторые из которых являются общими для концептуальных. Таким образом, осеменение может включать «затравку», ведущую к материнской иммунной толерантности, необходимой для выживания полуаллогенного концептуса [14, 9].
Воспалительные явления, которые, как известно, происходят при осеменении, могут также оказывать последующее влияние на процессы, важные для развития эмбриона, имплантации и инвазии трофобластов.Существенные изменения в цитокиновой среде яйцевода и матки, как следствие воздействия семенной плазмы, также могут способствовать усилению предимплантационного развития эмбриона и облегчению изменений как эпителия матки, так и стромы, необходимых для прикрепления и имплантации эмбриона. Эти ранние шаги в установлении беременности имеют решающее значение для постоянного успеха беременности.
Здесь мы суммируем текущее понимание событий на ранних сроках беременности и обсуждаем их возможную модуляцию воздействием на матку семенных факторов.На многие процессы, происходящие на ранних сроках беременности, по-видимому, влияют цитокины или лейкоциты, активируемые посредством передачи сигналов семенного фактора в женском тракте (рис.). Как следствие, нарушение контакта с семенами может иметь негативные последствия для событий, происходящих на ранних сроках беременности, что приводит к пагубным последствиям как для беременности, так и для потомства.
Схематическое изображение первых событий после осеменения. Компоненты семенной жидкости взаимодействуют с эпителием эндометрия с образованием эмбриотрофных факторов, поддерживающих эмбриональное развитие, а также цитокинов и хемокинов, вызывающих острую воспалительную реакцию.Инфильтрация лейкоцитов и антигенпрезентирующих клеток запускает иммунный ответ для успешного установления беременности и ремоделирования тканей для имплантации эмбриона. Все эти события имеют решающее значение для установления и поддержания здоровой беременности и инициируются воздействием семенной жидкости. Правая панель демонстрирует нашу гипотетическую серию событий, ведущих к изменению исходов беременности в отсутствие семенной жидкости. Отсутствие воспаления, вызванного семенной жидкостью, снижает продукцию эмбриотрофических факторов, иммунологическую толерантность к концептуальной части, минимальное ремоделирование тканей для облегчения имплантации и развития плаценты.Сочетание этих факторов приводит к нарушению программирования плода и развитию метаболического синдрома у взрослых
Раннее происхождение болезней у взрослых и программирование плода
Все чаще нарушения во внутриутробной среде связывают с изменением метаболического статуса и повышенным риском заболеваний во взрослой жизни. С конца 1980-х годов Дэвид Баркер и его коллеги определили четкую связь между низкой массой тела при рождении у людей и развитием гипертонии у взрослых [15].После этих первоначальных исследований серия эпидемиологических исследований показала связь между низкой массой тела при рождении и возникновением заболеваний у взрослых, включая гипертонию и вплоть до ожирения, сахарный диабет II типа, болезни сердца, болезни почек и синдром инсулинорезистентности (см. Обзор [16]). ). Взаимосвязь между массой тела при рождении и развитием болезни у взрослых получила название «зародышевые истоки болезни у взрослых». Потенциал роста плода контролируется на многих уровнях; однако одним из очень важных факторов является внутриутробная материнская среда.Ограничение кормления матери из-за экспериментальных подходов или нехватки продовольствия, как голод в Голландии во время Второй мировой войны, коррелировало с низкой массой тела при рождении и последующими изменениями эндокринных, метаболических и репродуктивных параметров у этих потомков в более позднем возрасте, а также с предрасположенностью. к некоторым видам рака [17–26]. Предполагается, что эти изменения эндокринных и метаболических параметров, по сути, программируют у потомства развитие эндокринно-ассоциированных заболеваний взрослых.
Молекулярные механизмы, лежащие в основе программирования плода, четко не определены. Однако в последнее время становится все более очевидным, что определенную роль может играть эпигенетическая регуляция генома [27]. На самых ранних стадиях эмбрионального развития эпигенетическая модификация концептуса может модулироваться эндогенными, экологическими и диетическими факторами. Митохондриальные аномалии также были предложены как механизмы, влияющие на программирование плода, как это было предложено исследованиями, изучающими митохондриальные аномалии, возникающие из-за культивирования эмбрионов in vitro [28, 29].Теперь было показано, что у потомства крыс, получавших диету с высоким содержанием жиров, не только нарушался гомеостаз глюкозы, но и снижалось количество митохондрий, что сопровождалось снижением экспрессии специфичных для митохондрий генов [29].
Пренатальное программирование эндокринных осей также является регулятором бочонка будущего здоровья и метаболического статуса последующего потомства. Считается, что оси гипоталамуса / гипофиза / надпочечников (HPA), соматотропа и инсулина вносят вклад в дифференциальную регуляцию ключевых эндокринных регуляторов метаболизма, которые могут влиять на метаболический статус человека.Эти высоко регулируемые тканеспецифические эндокринные регуляторы, как известно, находятся под влиянием программных механизмов, вызывающих дифференцированное развитие плода [30–32]. Совсем недавно было показано, что прямой вклад отца влияет на метаболизм потомства. Самцы крыс, получавшие диету с высоким содержанием жиров, дают потомство самок с дисфункцией β-клеток [33], в то время как наши собственные исследования доказывают, что самцы мышей, лишенные семенной плазмы, дают потомство самцов с измененным метаболическим профилем и повышенным накоплением жира [13]. .
Развитие эмбриона перед имплантацией
Эмбрион перед имплантацией чрезвычайно чувствителен к стрессовым факторам окружающей среды, таким как активные формы кислорода, аммоний и подача метаболического субстрата, поэтому небольшие нарушения в среде яйцевода / матки, в которой развивается эмбрион, могут иметь длительный период времени. срок воздействия на здоровье и жизнеспособность организма [34–36]. Прогресс от одноклеточной зиготы к дифференцированной, высокоорганизованной компетентной бластоцисте контролируется как материнскими, так и эмбриональными факторами.
Было показано, что специфические факторы роста и цитокины, экспрессируемые эпителием яйцевода и матки, имеют решающее значение для оптимального эмбрионального развития. Предполагается, что основным механизмом контроля экспрессии этих молекул являются стероидные гормоны яичников [37]. В последнее время регуляция этих факторов также приписывалась мужским факторам, полученным из спермы [38, 39]. Широкий спектр молекул, включая гранулоцитарный макрофагально-колониестимулирующий фактор (GM-CSF) [40], фактор ингибирования лейкемии (LIF) [41], IL-6, TGFβ, TNFα [42], TGFα [43], инсулин, инсулин. -подобный фактор роста (IGF) -I и II [44], эпидермальный фактор роста (EGF) [45] и гепарин-связывающий эпидермальный фактор роста-подобный фактор роста (HB-EGF) [46] были идентифицированы как имеющие потенциальные роли в эмбриональном развитии и частично регулируются в эпителии яйцевода за счет воздействия семенной плазмы.У самок мышей, спариваемых с самцами, лишенными семенной плазмы, экспрессия эмбриотрофных факторов в яйцеводе снижается, тогда как проапоптотический фактор Trail увеличивается. Кроме того, у эмбрионов, полученных в результате этих спариваний, наблюдаются нарушения в формировании бластоцист, которые могут быть частично устранены с помощью культивирования in vitro [13]. Окончательное исследование Sjoblom et al. продемонстрировал, что добавление GM-CSF в питательную среду может смягчить некоторые пагубные эффекты культивирования эмбрионов на исходы беременности, такие как изменение морфогенеза плаценты [47].Добавление многих этих эмбриотрофных факторов роста в культуральную среду для эмбрионов in vitro в настоящее время более тщательно исследуется на предмет их использования при вспомогательной репродукции человека, чтобы обеспечить более точную имитацию среды in vivo.
Семенная плазма
Осеменение
Осеменение — это доставка спермы в женские половые пути. При эякуляции мужчины производят примерно 4 мл спермы, которая содержит до 600 миллионов сперматозоидов. После коитуса эти сперматозоиды должны пройти по женскому тракту к ооциту, где может произойти оплодотворение.Эякулированная сперма содержит ряд компонентов, как клеточных, так и бесклеточных. В первую очередь, сперма рассматривается как концентрированная жидкость зрелой спермы. Однако сперма также содержит ряд эпителиальных и миелоидных клеток, происходящих из яичек и слизистой оболочки мочеполовой системы. Преобладающим компонентом спермы является семенная жидкость, называемая семенной плазмой. Семенная плазма получена из мужских дополнительных половых желез, включая железы семенных пузырьков, предстательную железу, придаток яичка и бульбоуретральную железу (или железу Кауперса).Жидкость, в которой сперма транспортируется через мужской мочеполовой тракт в женский репродуктивный тракт, богата белком и содержит ряд соединений, которые помогают поддерживать жизнеспособность сперматозоидов. Семенная плазма богата фруктозой, которая является преобладающим метаболическим субстратом, который способствует перемещению сперматозоидов через мужской мочеполовой тракт через шейку матки в яйцевод. Однако семенная жидкость также содержит ряд питательных микроэлементов и аминокислот, которые помогают удовлетворить высокие метаболические потребности сперматозоидов.Семенная плазма также является богатым источником как окислительных, так и антиоксидантных агентов. Было показано, что сперматозоиды очень чувствительны к окислительному повреждению ДНК из-за небольшой степени буферизации их уменьшенной цитоплазмы. Окислительный стресс возникает из-за присутствия гидроксильных радикалов, супероксид-анионов и перекиси водорода, присутствующих либо в эякуляте, либо в жидкостях женских половых путей. В случае повреждения ДНК сперматозоидов, в том числе вследствие окислительного стресса, может наступить срыв беременности или патологии из-за гибели эмбриона [48, 49].Чтобы противодействовать пагубному воздействию этих окислительных агентов, семенная плазма богата мощными антиоксидантными агентами, такими как каталаза и супероксиддисмутаза [50]. Семенная плазма обладает мощной буферной способностью, необходимой для противодействия жесткой кислой среде женских половых путей [51, 52].
Семенная плазма богата множеством активных белковых фрагментов. Было показано, что в семенной плазме человека и грызунов присутствуют различные сигнальные молекулы, в том числе многие из первоначально описанных по их иммунологической активности, включая TGFβ, интерферон-гамма (IFNγ), простагландин E 2 (PGE 2 ), некроз опухоли. фактор-альфа (TNFα) и члены семейства цитокинов интерлейкинов (IL), включая IL-1b, IL-6, IL-8, IL-10 и IL-12.TGFβ продуцируется преимущественно семенными пузырьками и присутствует в эякулированной семенной плазме в концентрации примерно 200 нг / мл, что значительно выше, чем в плазме крови [9]. Также известно, что семенные пузырьки мужчин продуцируют огромное количество PGE 2 , в результате чего уровни в семенной плазме в 100 000 раз превышают уровни, наблюдаемые в тканях во время острых воспалительных реакций [53]. Недавно стало очевидно, что функция этих молекул состоит в том, чтобы вызывать сильные молекулярные и клеточные реакции в женских половых путях после оплодотворения.
В течение десятилетий предполагалось, что единственной целью семенной плазмы является транспортная среда для сперматозоидов через женские репродуктивные пути. Однако совсем недавно были описаны дополнительные функции семенной плазмы во время установления и развития беременности, в частности, модуляция материнского иммунного ответа на беременность. Влияние удаления семенных пузырьков на фертильность было частично задокументировано у домашней мыши и золотого хомяка [54–56]. Peitz et al.продемонстрировали, что удаление семенных пузырьков сильно снижает способность этих мышей эффективно оплодотворять ооциты, что значительно снижает частоту наступления беременности у спарившихся самок. Аналогичным образом было показано, что хомячки-самцы, у которых были удалены добавочные железы, оказывают пагубное влияние на эмбриональное развитие [4, 57, 58].
Воспаление после осеменения
Индукция провоспалительных цитокинов является первым шагом в возникновении временной воспалительной реакции.Воспалительная реакция, возникающая при осеменении, может быть связана с факторами семенной плазмы, а не со спермой. Этот вывод основан на результатах, которые показывают отсутствие воспалительной реакции матки после спаривания мышей с самцами-кобелями с дефицитом семенных пузырьков [8], предполагая, что факторы, запускающие этот воспалительный каскад, происходят в семенных пузырьках, где вырабатывается большая часть семенной плазмы. . Повышающая регуляция цитокинов в шейке матки человека и мыши была специфически связана с цитокином семенной плазмы TGFβ [7, 11].
Воспалительная реакция, инициированная в шейке матки человека и матке мыши, очень похожа на классическую воспалительную реакцию, например, наблюдаемую после химического воздействия или травмы [59]. После того, как эпителиальные клетки матки подвергаются воздействию семенных факторов, выброс провоспалительных цитокинов и хемокинов (как указано выше) вызывает инфильтрацию воспалительных лейкоцитов. Помимо нейтрофилов, большое количество антигенпрезентирующих клеток (APC) рекрутируется в эндометрий матки, включая макрофаги и дендритные клетки (DC), экспрессирующие высокие уровни MHC класса II [60, 8].Этот ответ теперь хорошо охарактеризован у других видов, включая кроликов, лошадей, свиней и человека [61–64, 12].
Иммунологическое действие семенной плазмы
Как уже говорилось ранее, семенная плазма сама по себе обладает иммунными отклоняющими свойствами, некоторые из которых могут быть более важными, чем только защита сперматозоидов. Уже несколько десятилетий известно, что семенная плазма различных видов может напрямую влиять на иммунологические функции Т-клеток, В-клеток, NK-клеток и макрофагов in vitro [65–67].Хотя семенная жидкость напрямую не влияет на образование толерогенных лимфоцитов, было показано, что семенная жидкость нарушает комплемент-зависимый лизис клеток антител и клеточно-опосредованное уничтожение патогенных бактерий [68]. Андерсон и др. протестировали влияние семенной плазмы на степень гуморального ответа на провокацию антигеном у мышей и показали, что все фракции семенной плазмы; простата, семенные пузырьки и придатки яичка были способны подавлять как первичный, так и вторичный гуморальный ответ на введенную в вену отмытую сперму [69].Келли также продемонстрировал, что семенная плазма человека вызывает переключение цитокинов в лимфоцитах крови in vitro, что приводит к усилению регуляции IL-10 и понижению регуляции IL-12, эффективно создавая иммуносупрессивную среду [70].
Недавно было продемонстрировано, что семенная плазма, в которой преобладает биоактивный фактор TGFβ, обладает способностью взаимодействовать с женским трактом. Семенные жидкости нацелены на слой эпителиальных клеток шейки матки и матки, вызывая экспрессию провоспалительных цитокинов, таких как GM-CSF, CSF-1 (колониестимулирующий фактор 1), IL-1α, IL-6, IL-8, LIF. , RANTES и MIP-1α [9].Повышенная регуляция этих цитокинов эпителием имеет множество последствий. Эти провоспалительные цитокины ответственны за формирование воспалительной реакции после осеменения, в то время как многие цитокины также являются мощными иммунными отклоняющими сигналами, которые действуют, чтобы управлять созданием иммунной среды Th3, способствующей успеху беременности [71]. Известно, что другие цитокины, активируемые эпителием женского тракта в результате воздействия семенной плазмы, являются мощными эмбриотрофными молекулами.
Исследования на мышах показывают, что сперма играет роль в индукции системной иммунной толерантности на ранних сроках беременности. Самки, осемененные после перевязки матки, становятся временно толерантными к мужским трансплантационным антигенам, что измеряется по выживаемости после заражения отцовской опухолью, что позволяет предположить, что сперма, в отличие от самого эмбриона, является ключевым требованием для индукции толерантности [9]. Цитокиновая среда в месте воздействия антигена также является критическим фактором для будущего развития толерантности, и семенная плазма вызывает каскад событий, ведущих к индукции уникального цитокинового микроокружения с эпителием матки.
Антигенные характеристики спермы
Сперма несет множество отцовских антигенов, экспрессируемых в самой сперме, эпителиальных клетках половых путей и семенных лейкоцитах, некоторые из которых также экспрессируются концептусом [72, 73]. Количество антигенов, экспрессируемых на клетках трофобласта и обнаруживаемых в семенной жидкости, ограничено, однако существует ряд антигенов трансплантации, обнаруженных в семенной жидкости или экспрессированных в самой сперме. Было показано, что сперматозоиды мышей экспрессируют MHC классов I и II [74], а также H-Y [75], каждый из которых обладает потенциалом взаимодействовать с реактивными лимфоцитами и обычно экспрессируется концептусом.В случае человеческой спермы остается спорным вопрос, экспрессируются ли антигены MHC на поверхности сперматозоидов [76–78]. Однако очевидно, что в эякуляте также присутствует ряд лейкоцитов и эпителиальных клеток, которые, как было показано, экспрессируют антигены MHC [73].
Могут ли APC, набранные после осеменения, передаваться из матки в LN, еще предстоит официально продемонстрировать. Однако есть небольшое количество свидетельств того, что это действительно происходит. В середине 1970-х годов Бир и Биллингем показали, что PALN мышей временно увеличиваются после аллогенного осеменения, что указывает на приток клеток в PALN [79].Watson et al. показали, что радиоактивно меченные сперматозоиды, не участвующие в процессе оплодотворения, фагоцитируются макрофагами, экспрессирующими высокие уровни MHC класса II [80]. Уотсон также показал, что эти БТР могут передавать данные в MLN и селезенку; однако дренирующий LN матки в этом исследовании не исследовался. Parr et al. провели аналогичные исследования, используя введение FITC-конъюгированных белков для отслеживания поглощения антигена влагалищем и маткой мышей [81]. Parr et al. исследования показали, что введенные интравагинально белки позже локализовались в дендритных и лангерган-подобных клетках в эпителии и строме влагалища, тогда как меченые целые лимфоциты проходили через эпителий в ткань матери после введения в маточный тракт мыши [82].
Активация лимфоцитов после осеменения
Исследования, упомянутые выше, предполагают, что ЛУ в подвздошной кишке и ЛУ в матке являются дренирующими. Следовательно, можно предположить, что DC и макрофаги, выходящие из матки после оплодотворения, дойдут до этих LN и, возможно, станут участвовать в активации лимфоцитов. Совсем недавно было показано, что увеличение размера PALN происходит из-за притока или пролиферации клеток, и что активация Т-клеток, В-клеток и NK-клеток происходит после оплодотворения [83].Также было показано, что аллореактивные Т-клетки увеличивают количество в PALN мышей на ранних сроках беременности [84]. Хотя точный фенотип этих активированных лимфоцитов неизвестен, известно, что они рекрутируются обратно в ткани матки примерно во время имплантации, что предполагает их роль в подготовке иммунной среды матки к наступающей беременности [83]. Чтобы дополнительно подтвердить вывод, что материнская толерантность к отцовскому антигену происходит из этих LN, О’Хирн продемонстрировал, что клетки PALN, взятые от аллогенных беременных мышей, специфически гипочувствительны к отцовскому антигену по сравнению с таковыми от девственных или сингенных мышей [85].Также было продемонстрировано подавление аллореактивных Т-клеток, взятых из PALN во время предимплантационной и имплантационной стадий беременности, что в дальнейшем поддерживает оплодотворение как возможную отправную точку для толерантности материнских Т-клеток [86]. Клетки-супрессоры, продуцирующие TGFβ, также были идентифицированы в PALN во время имплантации [87]. Эксперименты, проведенные Beer et al. [88] показали, что удаление PALN перед спариванием уменьшало размер фетоплацентарной единицы у мышей, в то время как спленэктомия этого не делала, что согласуется с PALN, являющимся важным индуктивным участком материнской толерантности к полуаллогенному концептуалу.Совсем недавно важность антигенспецифических Т-регуляторных лимфоцитов (FoxP3 + / CD25 +) стала в центре внимания в поддержании беременности. Первоначальные исследования, истощающие Т-регуляторные лимфоциты, показали, что беременность не удается из-за иммунного отторжения концепта [89]. Наши исследования теперь показали, что воздействие семенной плазмы при осеменении вызывает увеличение Т-регуляторных лимфоцитов в PALN и матке [90].
Были предложены другие механизмы активации аллореактивных лимфоцитов, включая взаимодействие между лимфоцитами и антигеном в периферическом кровообращении за счет свободных клеток трофобласта в крови [91].Также был предложен механизм активации аллореактивных лимфоцитов самими клетками трофобласта [92].
Ремоделирование тканей и семенная плазма
Миелоидные иммунные клетки, рекрутируемые в матку после воздействия семенной плазмы, преимущественно макрофаги и нейтрофилы, могут играть роль в регуляции ремоделирования эпителия и стромы на ранних сроках беременности. Эти клетки играют ключевую роль в производстве молекул, критически важных для разрушения и регенерации определенных компонентов внеклеточного матрикса и образования новых кровеносных сосудов, которые, как известно, необходимы во время имплантации.
Макрофаги и нейтрофилы матки продуцируют ряд факторов, которые способствуют распаду и восстановлению ВКМ, а именно ММП и ТИМП. Нейтрофилы были идентифицированы как ключевой источник MMP-9, коллаген-специфической протеазы во время периимплантационного периода [93], в то время как макрофаги, как известно, продуцируют ряд MMP. Всестороннее исследование Chow et al. [94] на золотом хомяке показали, что экспрессия молекул, участвующих в ремоделировании ECM, контролируется во времени и пространстве и что семенная плазма участвует в их регуляции.VEGF, его рецепторы (VEGF-R1 и -R2) и экспрессия MMP-2 в матке во время периимплантационного периода все активировались воздействием семенной плазмы во время зачатия. Другое исследование дополнительно включило воздействие семенной плазмы на регулирование ремоделирования маточной артерии на ранних сроках беременности мышей, показав, что ремоделирование маточной артерии происходило сравнимо у мышей, спаривавшихся с вазэктомированными шпильками или интактными самцами-жеребцами [95].
Поверхностные характеристики эпителиальных клеток имеют первостепенное значение для успешного прикрепления эмбриона.Одно исследование продемонстрировало, что макрофаги могут вносить вклад в регуляцию адгезионных свойств эмбриона эпителиальных клеток in vitro [96]. Это предполагает дальнейшую важную роль макрофагов, рекрутируемых в ткани матки после воздействия семенной плазмы, уже на ранних этапах прикрепления эмбриона.
Семенная плазма и патологии беременности
Очевидно, что аномальные материнские иммунные реакции, особенно недостаточная иммунная толерантность, вредны для успеха беременности.Иммунные нарушения могут быть наиболее убедительно связаны с неудачей имплантации и отторжением трофобластов у женщин [97], которые являются основой патологий беременности, таких как преэклампсия и рецидивирующий самопроизвольный аборт. Имеются убедительные доказательства того, что сильный ответ Th2, ведущий к разрушительному клеточному иммунитету, вреден для исхода беременности [98], тогда как ответ Th3, приводящий к гуморальному иммунному ответу, рассматривается как более благоприятный для положительного исхода [99]. Считается, что общий фенотип и доля лимфоцитов также играют роль в таких патологиях, как самопроизвольный аборт.Например, NK-клетки линии Th2 связаны с резорбцией плода у мышей [98]. Интересно, что аберрантный иммунный ответ можно перенаправить; например, резорбция плода в модели мышей, склонных к аборту, значительно снижается за счет предварительной иммунизации самок материнскими клетками селезенки MHC класса II [100].
Другие иммунологические факторы, влияющие на беременность, по-видимому, связаны с воздействием спермы специфическим образом. Исследования на людях показывают, что как острое воздействие спермы в начале беременности, так и кумулятивное воздействие с течением времени могут защитить от повторного выкидыша и преэклампсии в зависимости от характера партнера [101].Исследования также показали, что воздействие спермы у женщин благоприятно сказывается на исходе беременности, использование барьерных методов контрацепции и период сожительства между парами позволяют предположить, что хроническое воздействие спермы на человека может быть полезным для последующих беременностей [102]. В настоящее время имеется большое количество доказательств того, что в этиологию преэклампсии вовлечены мужские факторы, происходящие из спермы [103, 104].
Семенная плазма и вспомогательная репродукция
Вспомогательные репродуктивные методы (ВРТ), такие как экстракорпоральное оплодотворение (ЭКО), стали широко используемым средством лечения бесплодия у людей.В настоящее время последствия такого лечения для здоровья потомства остаются спорными. Однако в настоящее время несколько исследований показывают, что беременность, вызванная ЭКО / ИКСИ, приводит к появлению у детей повышенного риска церебрального паралича [105], преждевременных родов [106, 107], низкой и очень низкой массы тела при рождении [108], осложнений во время родов. [109] и серьезные врожденные дефекты [110]. Однако важно отметить противоречие в современной литературе, где противоположные исследования не обнаружили связи между использованием АРТ и различными последствиями для здоровья у детей [111, 112].Механизмы возникновения этих изменений пока не определены; однако предполагается, что изменения эпигенетических генов плаценты и плода в результате возмущений периконцептуальной среды являются значимыми факторами [113].
Некоторые виды применения ВРТ относительно неинвазивны и частично имитируют естественное зачатие, например, внутриматочное оплодотворение. Однако высокотехнологичные подходы к ВРТ гораздо более инвазивны и кардинально отличаются от процесса естественного зачатия, особенно в том, что касается обращения с гаметами и эмбрионами.Обстоятельства, связанные с АРТ, сильно отличаются от естественного зачатия, включая использование неэякулированной спермы и принудительное оплодотворение путем внутрицитоплазматической инъекции сперматозоидов, а также культивирование эмбрионов in vitro в течение длительных периодов времени. Еще одним мешающим фактором при ВРТ является отсутствие контакта со спермой шейки матки как во время оплодотворения, так и при последующей имплантации.
Исследования на животных моделях начали изучать влияние воздействия спермы на изменение исхода переноса эмбриона.Carp et al. продемонстрировали, что механически индуцированные псевдобеременные крысы имели более высокую скорость имплантации после переноса эмбрионов при контакте со спермой во время имплантации [114]. Также было показано, что искусственное осеменение овец приносит пользу от воздействия плазмы семенной жидкости шейки матки, что приводит к увеличению процента беременных овец [6]. Удаление дополнительных половых желез у золотого хомячка показало значительное снижение экспрессии ангиогенных и эмбриотрофических факторов в периимплантационном эндометрии [94].Наши собственные исследования продемонстрировали восприимчивость очень ранних эмбрионов к рождению потомства с метаболическими нарушениями. Когда полученные in vivo двухклеточные эмбрионы переносятся в яйцевод, не подвергающийся воздействию семенной плазмы, у потомства развиваются метаболические фенотипы, тогда как полученные in vivo бластоцисты, перенесенные в ту же среду, не развиваются [13]. Совсем недавно эта работа была перенесена в программу АРТ. Было показано, что воздействие спермы во время переноса эмбриона увеличивает скорость имплантации эмбриона и возможное последующее развитие плода [5, 115, 116].Bellinge et al. ранее было показано, что воздействие семенной жидкости уже во время извлечения ооцитов может увеличить частоту наступления беременности у женщин, перенесших ЭКО [117]. Однако эффект непостоянен, поскольку аналогичные клинические испытания не выявили связи между высоким уровнем вагинального оплодотворения во время сбора ооцитов и частотой наступления беременности [118].
Резюме
В настоящее время существует большое количество доказательств, указывающих на важность воздействия семенной жидкости в стимулирование многофакторных изменений в материнской матке для создания среды, способствующей оптимальной имплантации эмбриона и исходу беременности.Многие из процессов, на которые, как известно, влияет воздействие семенной жидкости, имеют решающее значение для процессов раннего эмбрионального развития, имплантации и инвазии трофобластов. В современной литературе четко определено, что нарушение этих процессов может иметь пагубные последствия для потомства не только во время беременности, но и после рождения, с повышенным риском нарушений развития и обмена веществ. Хотя многие исследования были проведены на животных моделях, существуют эпидемиологические данные, свидетельствующие о важной роли воздействия семенной плазмы в профилактике патологий, связанных с беременностью, таких как преэклампсия и спонтанный повторный выкидыш.Это патологии с неясной этиологией; однако оба они связаны с нарушением иммунных изменений и другими критическими событиями, происходящими на очень ранних сроках беременности, в то время, когда известно, что воздействие семенной жидкости оказывает самое сильное влияние на репродуктивный тракт матери.
Благодарности
Я хотел бы поблагодарить Сару Робертсон, которая была пионером в этой области исследований и была поддерживающим наставником. Я также хотел бы поблагодарить Дэвида Альбертини за его поддержку и критическую оценку рукописи.
Сноски
Капсула Воздействие семенной жидкости способствует здоровому исходу беременности.
Ссылки
1. Queen K, Dhabuwala CB, Pierrepoint CG. Влияние удаления различных дополнительных половых желез на фертильность самцов крыс. J Reprod Fertil. 1981. 62 (2): 423–6. [PubMed] [Google Scholar] 2. Black CA, Rohan LC, Cost M, Watkins SC, Draviam R, Alber S и др. Слизистая оболочка влагалища служит индуктивным участком толерантности. J Immunol. 2000. 165 (9): 5077–83.[PubMed] [Google Scholar] 3. Cukierski MA, Sina JL, Prahalada S, Robertson RT. Влияние абляции семенных пузырьков и коагулирующих желез на фертильность крыс. Reprod Toxicol. 1991. 5 (4): 347–52. [PubMed] [Google Scholar] 4. Чан OC, Чоу PH, O WS. Полная абляция отцовских дополнительных половых желез снижает потенциал развития доимплантационных эмбрионов у золотистого хомяка. Анат Эмбриол (Берл). 2001. 204 (2): 117–22. [PubMed] 5. Тремеллен К.П., Вальбуэна Д., Ландерас Дж., Баллестерос А., Мартинес Дж., Мендоза С. и др.Влияние полового акта на частоту наступления беременности при искусственном оплодотворении человека. Hum Reprod. 2000. 15 (12): 2653–8. [PubMed] [Google Scholar] 6. Максвелл В.М., Эванс Г., Мортимер С.Т., Гиллан Л., Геллатли Е.С., Макфи, Калифорния. Нормальная фертильность овец после осеменения шейки матки замороженными-размороженными сперматозоидами с добавлением семенной плазмы. Reprod Fertil Dev. 1999. 11 (2): 123–6. [PubMed] [Google Scholar] 7. Тремеллен К.П., Seamark RF, Robertson SA. Семенной трансформирующий фактор роста бета1 стимулирует производство колониестимулирующего фактора гранулоцитов-макрофагов и рекрутирование воспалительных клеток в матке мышей.Биол Репрод. 1998. 58 (5): 1217–25. [PubMed] [Google Scholar] 8. Робертсон С.А., Мау В.Дж., Тремеллен К.П., Seamark RF. Роль высокомолекулярных белков семенных пузырьков в возникновении воспалительной реакции матки на сперму у мышей. J Reprod Fertil. 1996. 107 (2): 265–77. [PubMed] [Google Scholar] 9. Робертсон С.А., Мау В.Дж., Хадсон С.Н., Тремеллен К.П. Цитокин-лейкоцитарные сети и установление беременности. Am J Reprod Immunol. 1997. 37 (6): 438–42. [PubMed] [Google Scholar] 10. Робертсон С.А., Принс-младший, Шарки Д.И., Молденхауэр Л.М.Семенная жидкость и генерация регуляторных Т-клеток для имплантации эмбриона. Am J Reprod Immunol. 2013; 69 (4): 315–30. [PubMed] [Google Scholar] 11. Sharkey DJ, Macpherson AM, Tremellen KP, Mottershead DG, Gilchrist RB, Robertson SA. TGF-бета опосредует передачу сигналов провоспалительной семенной жидкости в эпителиальных клетках шейки матки человека. J Immunol. 2012. 189 (2): 1024–35. [PubMed] [Google Scholar] 12. Шарки Диджей, Тремеллен К.П., Джаспер М.Дж., Гемцелл-Даниэльссон К., Робертсон С.А. Семенная жидкость индуцирует набор лейкоцитов и экспрессию мРНК цитокинов и хемокинов в шейке матки человека после коитуса.J Immunol. 2012. 188 (5): 2445–54. [PubMed] [Google Scholar] 13. Бромфилд Дж. Дж., Шенкен Дж. Э., Чин П. Я., Care AS, Джаспер М. Дж., Робертсон С. А.. Факторы материнского тракта способствуют влиянию отцовской семенной жидкости на метаболический фенотип у потомства. Proc Natl Acad Sci U S. A. 2014; 111 (6): 2200–5. [Бесплатная статья PMC] [PubMed] [Google Scholar] 14. Tremellen KP. Семенной прайминг для успешной беременности у млекопитающих. В: Гупта С., редактор. Репродуктивная иммунология. Нью-Дели: Издательство Нароса; 1999. С. 88–96. [Google Scholar] 15.Баркер Д. Д., Осмонд С., Голдинг Дж., Кух Д., Уодсворт М. Е.. Рост в утробе матери, артериальное давление в детстве и взрослой жизни и смертность от сердечно-сосудистых заболеваний. Bmj. 1989. 298 (6673): 564–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 16. Баркер DJ. Матери, младенцы и здоровье в дальнейшей жизни. Эдинбург, Нью-Йорк: Черчилль Ливингстон; 1998. [Google Scholar] 17. Roseboom TJ, van der Meulen JH, Ravelli AC, Osmond C, Barker DJ, Bleker OP. Влияние пренатального воздействия голландского голода на заболеваемость взрослыми в более позднем возрасте: обзор.Mol Cell Endocrinol. 2001. 185 (1–2): 93–8. [PubMed] [Google Scholar] 18. Kind KL, Робертс CT, Sohlstrom AI. Katsman A. Robinson JS et al. Хроническое ограничение кормления матери замедляет рост, но увеличивает ожирение плода морской свинки. Am J Physiol Regul Integr Comp Physiol: Clifton PM; 2004. [PubMed] [Google Scholar] 19. Десаи М., Гейл Д., Бабу Дж., Росс М.Г. Запрограммированное ожирение у новорожденных с ограничением внутриутробного роста: модуляция питанием новорожденных. Am J Physiol Regul Integr Comp Physiol. 2005. 288 (1): R91–6.[PubMed] [Google Scholar] 20. Робинсон Дж. С., Фальконер Дж., Оуэнс Дж. А. Задержка внутриутробного развития: клиника и эксперимент. Acta Paediatr Scand Suppl. 1985; 319: 135–42. [PubMed] [Google Scholar] 21. Элиас С.Г., Петерс PH, Grobbee DE, van Noord PA. Риск рака груди после ограничения калорийности во время голода 1944–1945 годов в Голландии. J Natl Cancer Inst. 2004. 96 (7): 539–46. [PubMed] [Google Scholar] 22. Элиас С.Г., Петерс PH, Grobbee DE, van Noord PA. Голландский голод 1944–1945 гг. И последующая общая заболеваемость раком.Биомаркеры эпидемиологии рака Пред. 2005. 14 (8): 1981–5. [PubMed] [Google Scholar] 23. Элиас С.Г., ван Норд П.А., Петерс PH, ден Тонкелаар I, Гробби, DE. Воздействие голода в Голландии 1944–1945 годов в детстве и последующая репродуктивная функция женщин. Hum Reprod. 2005. 20 (9): 2483–8. [PubMed] [Google Scholar] 24. Добрый К.Л., Клифтон П.М., Кацман А.И., Циунис М., Робинсон Дж. С., Оуэнс Дж. А. Ограниченный рост плода и реакция на пищевой холестерин у морских свинок. Am J Physiol. 1999; 277 (6, часть 2): R1675–82. [PubMed] [Google Scholar]25.Белобраджич Д., Макинтош Г., Оуэнс Дж. Влияние пищевого белка на рост крыс, состав тела и чувствительность к инсулину. Азия Пак Дж. Клин Нутр. 2003; 12 Приложение: S42.
26. Квонг Вайоминг, Вайлд А.Е., Робертс П., Уиллис А.С., Флеминг Т.П. Недоедание матери в предимплантационный период развития крыс вызывает аномалии бластоцисты и программирование постнатальной гипертензии. Разработка. 2000. 127 (19): 4195–202. [PubMed] [Google Scholar] 27. Ву Джи, Базер Ф.В., Кадд Т.А., Майнингер С.Дж., Спенсер Т.Е. Питание матери и внутриутробное развитие.J Nutr. 2004. 134 (9): 2169–72. [PubMed] [Google Scholar] 28. McConnell JM, Petrie L. Оборот митохондриальной ДНК происходит во время доимплантационного развития и может регулироваться факторами окружающей среды. Репродукция Биомед онлайн. 2004. 9 (4): 418–24. [PubMed] [Google Scholar] 29. Taylor PD, McConnell J, Khan I.Y, Holemans K, Lawrence KM, Asare-Anane H, et al. Нарушение гомеостаза глюкозы и митохондриальные аномалии у потомства крыс, получавших во время беременности богатую жирами диету. Am J Physiol Regul Integr Comp Physiol.2005; 288 (1): R134–9. [PubMed] [Google Scholar] 30. Sayer AA, Cooper C. Плодотворное программирование состава тела и опорно-двигательного аппарата. Early Hum Dev. 2005. 81 (9): 735–44. [PubMed] [Google Scholar] 31. Фоуден А.Л., Форхэд А.Дж. Эндокринные механизмы внутриматочного программирования. Репродукция. 2004. 127 (5): 515–26. [PubMed] [Google Scholar] 32. Фоуден А.Л., Джуссани Д.А., Форхэд А.Дж. Эндокринное и метаболическое программирование во время внутриутробного развития. Early Hum Dev. 2005. 81 (9): 723–34. [PubMed] [Google Scholar] 33.Нг С.Ф., Лин Р.С., Лейбутт Д.Р., Баррес Р., Оуэнс Дж. А., Моррис М.Дж. Хроническая диета с высоким содержанием жиров у отцов программирует дисфункцию бета-клеток у потомства самок крыс. Природа. 2010. 467 (7318): 963–6. [PubMed] [Google Scholar] 34. Гарднер Д.К., Лейн М. Раннее развитие эмбриона ex vivo и влияние на экспрессию генов и импринтинг. Reprod Fertil Dev. 2005. 17 (3): 361–70. [PubMed] [Google Scholar] 35. Lane M, Gardner DK. Аммоний вызывает аберрантную дифференцировку бластоцисты, метаболизм, регуляцию pH, экспрессию генов и впоследствии изменяет развитие плода у мышей.Биол Репрод. 2003. 69 (4): 1109–17. [PubMed] [Google Scholar] 36. Lane M, Gardner DK. Понимание клеточных нарушений во время раннего развития эмбриона, которые нарушают жизнеспособность и развитие плода. Reprod Fertil Dev. 2005. 17 (3): 371–8. [PubMed] [Google Scholar] 37. Робертсон С.А., Майрхофер Дж., Симарк РФ. Стероидные гормоны яичников регулируют синтез колониестимулирующего фактора гранулоцитов-макрофагов эпителиальными клетками матки у мышей. Биол Репрод. 1996. 54 (1): 183–96. [PubMed] [Google Scholar] 38. Робертсон С.А.Фактор, стимулирующий колонии гранулоцитов-макрофагов (GM-CSF): паракринный регулятор в предимплантационной матке мыши. Аделаида: Университет Аделаиды; 1993. [Google Scholar] 39. Сджоблом С., Викланд М., Робертсон С.А. Колониестимулирующий фактор гранулоцитов-макрофагов (GM-CSF) действует независимо от общей бета-субъединицы рецептора GM-CSF, предотвращая апоптоз внутренней клеточной массы эмбрионов человека. Биол Репрод. 2002. 67 (6): 1817–23. [PubMed] [Google Scholar] 40. Робертсон С.А., Сджоблом К., Джаспер М.Дж., Норман Р.Дж., Seamark RF.Гранулоцитарно-макрофагальный колониестимулирующий фактор способствует транспорту глюкозы и жизнеспособности бластомеров у мышиных доимплантационных эмбрионов. Биол Репрод. 2001. 64 (4): 1206–15. [PubMed] [Google Scholar] 41. Lavranos TC, Rathjen PD, Seamark RF. Трофические эффекты фактора ингибирования миелоидного лейкоза (LIF) на эмбрионы мышей. J Reprod Fertil. 1995. 105 (2): 331–8. [PubMed] [Google Scholar] 42. Харди К., Спанос С. Экспрессия и функция фактора роста в преимплантационных эмбрионах человека и мыши. J Endocrinol. 2002. 172 (2): 221–36.[PubMed] [Google Scholar] 43. Шульц Г.А., Хейнер С. Факторы роста в доимплантационных эмбрионах млекопитающих. Oxf Rev Reprod Biol. 1993; 15: 43–81. [PubMed] [Google Scholar] 44. Харви МБ, Кэй ПЛ. Опосредование действий инсулина и инсулиноподобного фактора роста-1 на доимплантационных эмбрионах мышей in vitro. Mol Reprod Dev. 1992. 33 (3): 270–5. [PubMed] [Google Scholar] 45. Брайс Э. К., Ву Дж. Х., Мураро Р., Адамсон Э. Д., Уайли Л. М.. Модуляция предимплантационного развития мышей антителами к рецепторам эпидермального фактора роста, антисмысловой РНК и дезоксиолигонуклеотидами.Dev Genet. 1993. 14 (3): 174–84. [PubMed] [Google Scholar] 46. Tamada H, Higashiyama C, Takano H, Kawate N, Inaba T., Sawada T. Влияние гепарин-связывающего эпидермального фактора роста, подобного фактору роста, на доимплантационное развитие эмбриона и имплантацию крысе. Life Sci. 1999. 64 (22): 1967–73. [PubMed] [Google Scholar] 47. Сджоблом С., Робертс СТ, Викланд М., Робертсон С.А. Гранулоцитарно-макрофагальный колониестимулирующий фактор смягчает неблагоприятные последствия культивирования эмбрионов на траекторию роста плода и морфогенез плаценты.Эндокринология. 2005. 146 (5): 2142–53. [PubMed] [Google Scholar] 48. Эйткен Р.Дж., Бейкер М.А., Сойер Д. Окислительный стресс в мужской зародышевой линии и его роль в этиологии мужского бесплодия и генетических заболеваний. Репродукция Биомед онлайн. 2003. 7 (1): 65–70. [PubMed] [Google Scholar] 49. Саноцка Д., Мизель Р., Енджейчак П., Хелмонска-Сойта А.С., Курпиш М. Влияние активных форм кислорода и активность антиоксидантных систем на сперму человека; ассоциация с мужским бесплодием. Инт Дж. Андрол. 1997. 20 (5): 255–64. [PubMed] [Google Scholar] 50.Гарридо Н., Месегер М., Саймон С., Пеллисер А., Ремохи Дж. Прооксидативный и антиоксидантный дисбаланс в сперме человека и его связь с мужской фертильностью. Азиат Дж. Андрол. 2004. 6 (1): 59–65. [PubMed] [Google Scholar] 51. Wolters-Everhardt E, Dony JM, Lemmens WA, Doesburg WH, De Pont JJ. Буферная способность спермы человека. Fertil Steril. 1986. 46 (1): 114–9. [PubMed] [Google Scholar] 52. Вольтерс-Эверхардт Э., Дони Дж. М., Питерс У. С., Де Пон Дж. Дж. Буферные вещества спермы человека. Fertil Steril. 1987. 48 (1): 159–61. [PubMed] [Google Scholar] 53.Келли РУ. Простагландины в сперме приматов: смещение иммунной системы в пользу сперматозоидов и вирусов? Простагландины Leukot Essent Fatty Acids. 1997. 57 (2): 113–8. [PubMed] [Google Scholar] 54. Пейтц Б., Олдс-Кларк П. Влияние удаления семенных пузырьков на фертильность и подвижность маточных сперматозоидов у домашней мыши. Биол Репрод. 1986. 35 (3): 608–17. [PubMed] [Google Scholar] 55. Инь И, Чоу PH. Чунг МП. О WS. Влияние дополнительных половых желез самцов на деконденсацию спермы и активацию ооцитов во время оплодотворения in vivo у золотистых хомяков.Инт Дж. Андрол. 1999; 22: 68–76. [PubMed] [Google Scholar] 56. Панг С.Ф., Чоу PH, Вонг TM. Роль семенных пузырьков, коагулирующих желез и предстательной железы на фертильность и плодовитость мышей. J Reprod Fertil. 1979; 56 (1): 129–32. [PubMed] [Google Scholar] 57. WS O, Chen HQ, Chow PH. Влияние секреции дополнительных половых желез самцов на раннее эмбриональное развитие золотистого хомячка. J Reprod Fertil. 1988. 84 (1): 341–34. [PubMed] [Google Scholar] 58. Цзян Х.Й., О WS, Ли К. Х., Тан П.Л., Чоу PH. Удаление отцовских дополнительных половых желез вредно для развития эмбриона во время имплантации.Анат Эмбриол (Берл). 2001. 203 (4): 255–63. [PubMed] 59. Де М. Определение количества и распределения макрофагов, лимфоцитов и гранулоцитов в матке мыши от спаривания посредством имплантации. J Leukoc Biol. 1991; 50: 252–62. [PubMed] [Google Scholar] 60. Томпсон Л.А., Баррат К.Л., Болтон А.Е., Кук И.Д. Лейкоцитарная реакция шейки матки человека. Am J Reprod Immunol. 1992. 28 (2): 85–9. [PubMed] [Google Scholar] 61. Филлипс Д.М., Малер С. Эмиграция и миграция лейкоцитов во влагалище после спаривания у кролика.Анат Рек. 1977; 189 (1): 45–59. [PubMed] [Google Scholar] 62. О’Лири S, Джаспер MJ, Warnes GM, Armstrong DT, Robertson SA. Семенная плазма регулирует экспрессию цитокинов эндометрия, рекрутирование лейкоцитов и развитие эмбриона свиньи. Репродукция. 2004. 128 (2): 237–47. [PubMed] [Google Scholar] 63. Пандья И.Дж., Коэн Дж. Лейкоцитарная реакция шейки матки человека на сперматозоиды. Fertil Steril. 1985. 43 (3): 417–21. [PubMed] [Google Scholar] 64. Троедссон М.Х., Лосет К., Альгамди А.М., Дамс Б., Крабо Б.Г.Взаимодействие между спермой лошадей и эндометрием: воспалительная реакция на сперму. Anim Reprod Sci. 2001. 68 (3–4): 273–8. [PubMed] [Google Scholar] 65. Андерсон DJ, Тартер TH. Иммуносупрессивные эффекты компонентов семенной плазмы мышей in vivo и in vitro. J Immunol. 1982; 128 (2): 535–9. [PubMed] [Google Scholar] 66. Фахми Х.А., Хантер АГ, Маркхэм Р.Дж., Сегин БЭ. Иммуносупрессивная активность семенной плазмы крупного рогатого скота на лимфоциты крупного рогатого скота in vitro. J Dairy Sci. 1985. 68 (9): 2315–21. [PubMed] [Google Scholar] 67.Саксена С., Джа П., Фарук А. Иммуносупрессия семенной плазмой человека. Иммунол Инвест. 1985. 14 (3): 255–69. [PubMed] [Google Scholar] 68. Джеймс К. Иммуносупрессия семенной плазмой и ее возможное клиническое значение. Иммунол сегодня. 1984. 5 (12): 357–63. [PubMed] [Google Scholar] 69. Андерсон DJ, Тартер TH. Иммуносупрессивные эффекты компонентов семенной плазмы мышей in vivo и in vitro. J Immunol. 1982; 128 (2): 535–9. [PubMed] [Google Scholar] 70. Келли Р.У., Карр Г.Г., Кричли ХО. Переключение цитокинов, индуцированное семенной плазмой человека: иммунная модуляция с последствиями для заболеваний, передающихся половым путем.Hum Reprod. 1997. 12 (4): 677–81. [PubMed] [Google Scholar] 71. Робертсон С., Шарки Д. Роль спермы в индукции материнской иммунной толерантности к беременности. Semin Immunol. 2001. 13 (4): 243–54. [PubMed] [Google Scholar] 72. Thaler CJ. Иммунологическая роль семенной плазмы при осеменении и беременности. Am J Reprod Immunol. 1989. 21 (3–4): 147–50. [PubMed] [Google Scholar] 73. Quayle AJ, Xu C, Mayer KH, Anderson DJ. Т-лимфоциты и макрофаги, но не подвижные сперматозоиды, являются важным источником вируса иммунодефицита человека в сперме.J Infect Dis. 1997. 176 (4): 960–8. [PubMed] [Google Scholar] 74. Уенояма МК. Коэволюция главного комплекса гистосовместимости и t-комплекса у мышей. I. Создание и поддержание ассоциаций высокой степени взаимодополняемости. Генетика. 1989. 121 (1): 139–51. [Бесплатная статья PMC] [PubMed] [Google Scholar] 75. Айер С.В., Нандедкар Т.Д., Hegde UC. Продукция антитела H-Y в асцитной жидкости мыши и локализация антигена на клетках и тканях. Gamete Res. 1989. 22 (1): 37–49. [PubMed] [Google Scholar] 76.Андерсон DJ, Бах DL, Юнис EJ, ДеВольф WC. Основные антигены гистосовместимости не экспрессируются в сперматозоиде придатка яичка человека. J Immunol. 1982. 129 (2): 452–4. [PubMed] [Google Scholar] 77. Hutter H, Dohr G. Экспрессия HLA на незрелых и зрелых половых клетках человека. J Reprod Immunol. 1998. 38 (2): 101–22. [PubMed] [Google Scholar] 78. Yao GD, Shu YM, Shi SL, Peng ZF, Song WY, Jin HX и др. Экспрессия и потенциальные роли HLA-G в сперматогенезе человека и раннем эмбриональном развитии. ПлоС один. 2014; 9 (3): e92889.[Бесплатная статья PMC] [PubMed] [Google Scholar] 79. Пиво AE, Billingham RE. Ответы хозяина на внутриматочные ткани, клеточные и фетальные аллотрансплантаты. J Reprod Fertil, Suppl. 1974; 21: 59–88. [Google Scholar] 80. Уотсон Дж. Г., Чайкин С., Кэрролл Дж. Восстановление у мышей: судьба спрематозоидов, не участвующих в оплодотворении. Gamete Res. 1983; 7: 75–84. [Google Scholar] 81. Парр М.Б., Парр Э.Л. Распознавание антигенов в женских половых путях: I. Поглощение внутрипросветных маркеров белка во влагалище мышей. J Reprod Immunol.1990. 17 (2): 101–14. [PubMed] [Google Scholar] 82. Парр Э.Л., Парр М.Б., Чжэн Л.М., Янг JD. Гранулированные клетки метриальной железы мыши возникают в результате локальной активации лимфоцитов-естественных киллеров матки. Биол Репрод. 1991; 44 (5): 834–41. [PubMed] [Google Scholar] 83. Йоханссон М., Бромфилд Дж. Дж., Джаспер М. Дж., Робертсон С. А.. Сперма активирует женский иммунный ответ на ранних сроках беременности у мышей. Иммунология. 2004. 112 (2): 290–300. [Бесплатная статья PMC] [PubMed] [Google Scholar] 84. Piazzon I, Matusevich M, Deroche A, Nepomnaschy I, Pasqualini CD.Раннее повышение реактивности трансплантат против хозяина во время беременности у мышей. J Reprod Immunol. 1985. 8 (2–3): 129–37. [PubMed] [Google Scholar] 85. О’Хирн М., Хилгард HR. Вызванные беременностью изменения в реактивности клеток маточного дренирования и периферических лимфатических узлов трансплантат против хозяина на аллоантигены плода. Трансплантация. 1981; 32 (5): 389–91. [PubMed] [Google Scholar] 86. Капович М., Рукавина Д. Кинетика лимфопролиферативных реакций лимфоцитов, собранных из лимфатических узлов матки во время беременности у крыс.J Reprod Immunol. 1991; 20: 93–101. [PubMed] [Google Scholar] 87. Кларк Д. Споры в репродуктивной иммунологии. Crit Rev Immunol. 1991. 11 (3,4): 215–47. [PubMed] 88. Пиво А.Э., Скотт-младший, Биллингем Р.Э. Гистосовместимость и материнский иммунологический статус как детерминанты веса плода и размера помета у грызунов. J Exp Med. 1975. 142 (1): 180–96. [Бесплатная статья PMC] [PubMed] [Google Scholar] 89. Алувихаре В.Р., Калликурдис М., Бец АГ. Регуляторные Т-клетки опосредуют материнскую толерантность к плоду. Nat Immunol.2004. 5 (3): 266–71. [PubMed] [Google Scholar] 90. Герин Л. Р., Молденхауэр Л. М., Принс Дж. Р., Бромфилд Дж. Дж., Хейболл Дж. Д., Робертсон С.А. Семенная жидкость регулирует накопление регуляторных Т-клеток FOXP3 + в матке мышей до имплантации посредством увеличения пула клеток FOXP3 + и CCL19-опосредованного рекрутирования. Биол Репрод. 2011. 85 (2): 397–408. [PubMed] [Google Scholar] 91. Ваккио М.С., Цзян С.П. Плод и материнская иммунная система: беременность как модель для изучения толерантности периферических Т-клеток. Crit Rev Immunol. 1999. 19 (5–6): 461–80.[PubMed] [Google Scholar] 92. Биллингем Р. Трансплантационный иммунитет и материнско-плодовые отношения. N Engl J Med. 1964; 270 (13): 667–71. [PubMed] [Google Scholar] 93. Даймон Э., Вада Ю. Роль нейтрофилов в активности матриксной металлопротеиназы в матке мышей до имплантации. Биол Репрод. 2005. 73 (1): 163–71. [PubMed] [Google Scholar] 94. Чоу PH, Цзян Х.Й., Пун Х.К., Ли К.Х., О. WS. Эмбрионы, полученные от самцов без дополнительных половых желез, вызывают отказ маточной поддержки: исследование экспрессии VEGF, MMP и TGF у золотистого хомячка.Анат Эмбриол (Берл). 2003. 206 (3): 203–13. [PubMed] 95. ван дер Хейден О.В., Эссерс Ю.П., Спандерман М.Э., Де Мей Дж.Г., ван Эйс Г.Дж., Петерс ЛЛ. Ремоделирование маточной артерии при псевдобеременности сопоставимо с таковым на ранних сроках беременности. Биол Репрод. 2005. 73 (6): 1289–93. [PubMed] [Google Scholar] 96. Косака К., Фудзивара Х., Тацуми К., Йошиока С., Хигучи Т., Сато Ю. и др. Мононуклеарные клетки периферической крови человека усиливают межклеточное взаимодействие между эпителиальными клетками эндометрия человека и сфероидами BeWo-клеток. Hum Reprod.2003. 18 (1): 19–25. [PubMed] [Google Scholar] 97. Hill JA. T-helper 1-type иммунитет к трофобласту: данные о новом иммунологическом механизме повторного аборта у женщин. Hum Reprod. 1995; 10 (Дополнение 2): 114–20. [PubMed] [Google Scholar] 98. Рагупати Р. Иммунитет по Th2-типу несовместим с успешной беременностью. Иммунол сегодня. 1997. 18 (10): 478–82. [PubMed] [Google Scholar] 99. Канбур А., Хо Х. Н., Мисра Д. Н., Макферсон Т. А., Кунц Х. В., Гилл Т. Дж.. Дифференциальная экспрессия антигенов MHC класса I на плаценте крысы.Механизм выживания аллотрансплантата плода. J Exp Med. 1987. 166 (6): 1861–82. [Бесплатная статья PMC] [PubMed] [Google Scholar] 100. Kiger N, Chaouat G, Kolb JP, Wegmann TG, Guenet JL. Иммуногенетические исследования самопроизвольного аборта на мышах. Преиммунизация самок аллогенными клетками. J Immunol. 1985. 134 (5): 2966–70. [PubMed] [Google Scholar] 101. Клонофф-Коэн Х.С., Савиц Д.А., Селафо Р.С., Макканн М.Ф. Эпидемиологическое исследование контрацепции и преэклампсии. Журнал Американской медицинской ассоциации.1989; 262: 3143–7. [PubMed] [Google Scholar] 102. Робиллард П.Ю., Халси Т.С., Перианин Дж., Янки Э., Мири Э.Х., Папирник Э. Связь гипертонии, вызванной беременностью, с продолжительностью полового сожительства до зачатия. Ланцет. 1995; 344: 973–5. [PubMed] [Google Scholar] 103. Деккер Г.А., Робиллард П.Й., Халси Т.К. Иммунная дезадаптация в этиологии преэклампсии: обзор подтверждающих эпидемиологических исследований. ObstetGynecolSurv. 1998. 53 (6): 377–82. [PubMed] [Google Scholar] 104. Робертсон С.А., Бромфилд Дж. Дж., Тремеллен К.П.Семенное «праймирование» для защиты от преэклампсии — объединяющая гипотеза. J Reprod Immunol. 2003. 59 (2): 253–65. [PubMed] [Google Scholar] 105. Ламберт РД. Проблемы безопасности при вспомогательных репродуктивных технологиях: этиология проблем со здоровьем у детей, рожденных после ВРТ. Hum Reprod. 2003. 18 (10): 1987–91. [PubMed] [Google Scholar] 106. Перри Т., Чен Р., Йоэли Р., Мерлоб П., Орвието Р., Шалев Ю. и др. Существует ли риск преждевременных родов при одноплодной беременности с применением вспомогательных репродуктивных технологий? J Assist Reprod Genet. 2001. 18 (5): 245–9.[Бесплатная статья PMC] [PubMed] [Google Scholar] 107. Ван Дж. Х, Норман Р. Дж., Кристианссон П. Влияние различных методов лечения бесплодия на риск преждевременных родов. Hum Reprod. 2002. 17 (4): 945–9. [PubMed] [Google Scholar] 108. Schieve LA, Meikle SF, Ferre C, Peterson HB, Jeng G, Wilcox LS. Низкая и очень низкая масса тела при рождении у младенцев, зачатых с использованием вспомогательных репродуктивных технологий. N Engl J Med. 2002. 346 (10): 731–7. [PubMed] [Google Scholar] 109. Ochsenkuhn R, Strowitzki T, Gurtner M, Strauss A, Schulze A, Hepp H, et al.Осложнения беременности, акушерские риски и неонатальный исход при одноплодной и многоплодной беременности после ПОДАРОК и ЭКО. Arch Gynecol Obstet. 2003. 268 (4): 256–61. [PubMed] [Google Scholar] 110. Хансен М., Куринчук Дж. Дж., Бауэр С., Уэбб С. Риск серьезных врожденных дефектов после интрацитоплазматической инъекции сперматозоидов и экстракорпорального оплодотворения. N Engl J Med. 2002. 346 (10): 725–30. [PubMed] [Google Scholar] 111. Маршан Э., Понселе С., Карбийон Л., Фаризиен I, Тигаизин А., Шанель О. Есть ли больше осложнений при беременности из-за вспомогательных репродуктивных технологий, чем при спонтанной беременности? Ретроспективное исследование более 6 лет.Журнал гинекологии, акушерства и биологии репродукции. 2011. 40 (6): 522–8. [PubMed] [Google Scholar] 112. Берри К.А., Барон И.С., Вайс Б.А., Бейкер Р., Аронович М.Д., Литман Ф.Р. Экстракорпоральное оплодотворение и нейропсихологические результаты поздних недоношенных дошкольников: исследование PETIT. Am J Obstet Gynecol. 2013; 209 (4): 356 e1-6. DOI: 10.1016 / j.ajog.2013.06.041. [PubMed] 113. Томпсон Дж. Г., Вид К. Л., Робертс К. Т., Робертсон С. А., Робинсон Дж. С.. Эпигенетические риски, связанные с вспомогательными репродуктивными технологиями: краткосрочные и долгосрочные последствия для здоровья детей, зачатых с помощью вспомогательных репродуктивных технологий: еще один повод для осторожности? Hum Reprod.2002. 17 (11): 2783–6. [PubMed] [Google Scholar] 114. Карп Х. Дж., Серр Д. М., Машиах С., Небель Л. Влияние осеменения на имплантацию перенесенных бластоцист крысы. Gynecol Obstet Invest. 1984. 18 (4): 194–8. [PubMed] [Google Scholar] 115. Кулам CB, Стерн JJ. Влияние семенной плазмы на частоту имплантации. Ранняя беременность. 1995; 1 (1): 33–6. [PubMed] [Google Scholar] 116. Маркони Г., Оуге Л., Осес Р., Кинтана Р., Раффо Ф., Янг Э. Улучшает ли половой акт уровень беременности при внутрифаллопиевом переносе гамет? Fertil Steril.1989. 51 (2): 357–9. [PubMed] [Google Scholar] 117. Беллиндж Б.С., Коупленд К.М., Томас Т.Д., Маццучелли Р.Э., О Нил Дж., Коэн М.Дж. Влияние оплодотворения пациента на частоту имплантации в программе экстракорпорального оплодотворения и переноса эмбрионов. Fertil Steril. 1986. 46 (2): 252–6. [PubMed] [Google Scholar] 118. Фишел С., Вебстер Дж., Джексон П., Фаратиан Б. Оценка высокой вагинальной инсеминации при извлечении ооцитов у пациентов, подвергающихся экстракорпоральному оплодотворению. Fertil Steril. 1989. 51 (1): 135–8. [PubMed] [Google Scholar]Мужская репродуктивная система (для родителей)
Что такое репродукция?
Размножение — это процесс, с помощью которого организмы делают больше организмов похожими на самих себя.Но даже несмотря на то, что репродуктивная система важна для поддержания жизни вида, в отличие от других систем организма, не обязательно поддерживать жизнь индивидуума.
В репродуктивном процессе человека участвуют два типа половых клеток, или гамет, (GAH-meetz). Мужская гамета, или сперматозоид, и женская гамета, яйцеклетка или яйцеклетка, встречаются в репродуктивной системе самки. Когда сперма оплодотворяет (встречает) яйцеклетку, эта оплодотворенная яйцеклетка называется зиготой (ZYE-коза). Зигота превращается в эмбрион и превращается в плод.
И мужская репродуктивная система, и женская репродуктивная система необходимы для воспроизводства.
Люди, как и другие организмы, передают некоторые характеристики себя следующему поколению. Мы делаем это через наши гены, особые носители человеческих качеств. Гены, передаваемые родителями, делают их детей похожими на других в семье, но также и делают каждого ребенка уникальным. Эти гены происходят из мужской спермы и женской яйцеклетки.
Что такое мужская репродуктивная система?
У самца репродуктивные органы или гениталии находятся как внутри, так и снаружи таза.К мужским гениталиям относятся:
- Яички (TESS-tih-kulz)
- Система протоков, состоящая из придатка яичка и семявыносящего протока
- Добавочные железы, которые включают семенные пузырьки и предстательную железу
- пенис
У парня, достигшего половой зрелости, два овальных яичек или яичек (TESS-teez) производят и хранят миллионы крошечных сперматозоидов. Яички также являются частью эндокринной системы, потому что они вырабатывают гормоны, в том числе тестостерон (tess-TOSS-tuh-rone).
Тестостерон — основная часть полового созревания у мальчиков, и по мере того, как парень проходит через половое созревание, его яички вырабатывают его все больше и больше. Тестостерон — это гормон, от которого у мальчиков развиваются более глубокие голоса, большие мышцы, а также волосы на теле и лице. Он также стимулирует выработку спермы.
Рядом с яичками находятся придатки яичка, и семявыносящие протоки, по которым проходит сперма. Эпидидимис (ep-uh-DID-uh-miss) и яички свешиваются в виде мешочка за пределами таза, называемого мошонкой .Этот мешок из кожи помогает регулировать температуру яичек, которые должны быть ниже температуры тела, чтобы производить сперму. Мошонка меняет размер, чтобы поддерживать нужную температуру. Когда тело холодное, мошонка сжимается и становится более плотной, чтобы удерживать тепло тела. В тепле он становится больше и мягче, чтобы избавиться от лишнего тепла. Это происходит, когда парню даже не нужно об этом думать. Мозг и нервная система дают мошонке сигнал изменить размер.
Дополнительные железы , включая семенных пузырьков и предстательную железу , обеспечивают жидкость, которая смазывает систему протоков и питает сперму.Уретра — это канал, по которому сперма (в жидкости, называемой спермой) выходит за пределы тела через половой член. Уретра также является частью мочевыделительной системы, потому что это также канал, через который проходит моча, покидая мочевой пузырь и покидая тело.
Пенис фактически состоит из двух частей: стержня и головки . Ствол — это основная часть полового члена, а головка — это кончик (иногда называемый головкой). В конце головки есть небольшая щель или отверстие, через которое сперма и моча выходят из тела через уретру (yoo-REE-thruh).Внутренняя часть полового члена состоит из губчатой ткани, которая может расширяться и сжиматься.
Все мальчики рождаются с крайней плотью , кожной складкой на конце полового члена, покрывающей головку. Некоторым мальчикам делают обрезание, что означает, что врач или священник отрезают крайнюю плоть. Обрезание обычно делают в первые несколько дней жизни мальчика. В этом нет необходимости с медицинской точки зрения, но родители, решившие сделать обрезание своим сыновьям, часто делают это на основании религиозных убеждений, соображений гигиены или культурных или социальных причин.Мальчики, которым сделали обрезание полового члена, и те, кто не сделал этого, ничем не отличаются: все пенисы работают и ощущаются одинаково, независимо от того, была ли удалена крайняя плоть.
Как работает мужская репродуктивная система?
Мужская репродуктивная система:
- производит сперму (SEE-mun)
- выпускает сперму в репродуктивную систему женщины во время полового акта
- производит половые гормоны, которые помогают мальчику развиться в половозрелого мужчину в период полового созревания
Когда рождается мальчик, у него есть все части репродуктивной системы, но только в период полового созревания он может воспроизводить потомство.Когда начинается половая зрелость, обычно в возрасте от 9 до 15 лет, возраст
гипофиз, расположенный рядом с мозгом, вырабатывает гормоны, которые стимулируют выработку тестостерона яичками. Производство тестостерона вызывает множество физических изменений.Хотя время этих изменений у каждого парня разное, стадии полового созревания обычно следуют установленной последовательности:
- На первом этапе полового созревания у мужчин мошонка и семенники увеличиваются в размерах.
- Далее половой член становится длиннее, а семенные пузырьки и предстательная железа разрастаются.
- Волосы начинают расти в области лобка, а затем на лице и подмышках. За это время голос мальчика также становится глубже.
- У мальчиков также наблюдается скачок роста в период полового созревания, когда они достигают своего взрослого роста и веса.
Что делают сперматозоиды?
Мужчина, достигший половой зрелости, будет производить миллионы сперматозоидов каждый день. Каждый сперматозоид чрезвычайно мал: всего 1/600 дюйма (0,05 миллиметра в длину). Сперматозоиды развиваются в яичках в системе крошечных трубок, которые называются семенными канальцами .При рождении эти канальцы содержат простые круглые клетки. Во время полового созревания тестостерон и другие гормоны заставляют эти клетки превращаться в сперматозоиды. Клетки делятся и изменяются, пока не получат голову и короткий хвост, как у головастиков. Голова содержит генетический материал (гены). Сперматозоиды попадают в придатки яичка, где они завершают свое развитие.
Затем сперматозоид перемещается к семявыносящему протоку (VAS DEF-uh-runz) или семявыносящему протоку. Семенные пузырьки и предстательная железа образуют беловатую жидкость, называемую семенной жидкостью, которая смешивается со спермой с образованием спермы при сексуальной стимуляции мужчины.Пенис, который обычно безвольно свисает, становится твердым, когда мужчина сексуально возбужден. Ткани полового члена наполняются кровью, и он становится жестким и эректильным (эрекция). Жесткость эрегированного полового члена облегчает введение во влагалище женщины во время секса. Когда эрегированный половой член стимулируется, мышцы вокруг репродуктивных органов сокращаются и выталкивают сперму через систему протоков и уретру. Сперма выталкивается из тела мужчины через уретру — этот процесс называется эякуляцией .Каждый раз, когда парень эякулирует, в нем может содержаться до 500 миллионов сперматозоидов.
Что такое зачатие?
Если сперма эякулирует во влагалище женщины, миллионы сперматозоидов «плывут» вверх из влагалища через шейку матки и матку, чтобы встретиться с яйцеклеткой в маточной трубе. Для оплодотворения яйцеклетки требуется всего один сперматозоид.
Эта оплодотворенная яйцеклетка теперь называется зиготой и содержит 46 хромосом — половину из яйца и половину из сперматозоидов. Генетический материал мужского и женского пола объединяется, так что можно создать новую особь.Зигота снова и снова делится по мере роста в матке самки, превращаясь в течение беременности в эмбрион, плод и, наконец, новорожденного ребенка.
| Введение: Сперма — это вещество, которое эякулирует самец и которое содержит сперму. Некоторые железы вносят свой вклад в семенную жидкость, поскольку сперма продвигается из семенных пузырьков в окружающую среду за пределами мужского тела. Средний объем эякулята — 3.4 мл со стандартным отклонением 1,62 мл. Объем уменьшается при повторном половом акте и может значительно увеличиться после длительного воздержания. Семенная жидкость слабощелочная (pH 7,2-7,4). Перед эякуляцией 1-2 капли прозрачной бесцветной жидкости, выделяемой бульбоуретральными железами, нейтрализуют кислотность уретры.Далее следует молочная секреция простаты, обычно без сперматозоидов, а затем часть со сперматозоидами. Наконец, появляется студенистый, вязкий секрет семенных пузырьков. Фруктоза происходит в основном из семенных пузырьков и, по-видимому, играет важную роль в качестве источника энергии для подвижности сперматозоидов в анаэробной среде женских половых путей (кислород токсичен для сперматозоидов). Фертильность: Нормальный объем спермы, по-видимому, важен для буферизации кислотности вагинального секрета.Подвижность сперматозоидов зависит от значения pH, и при контакте с кислым вагинальным секретом (pH 3,5-4,2) они быстро иммобилизуются. Слишком большой объем спермы разжижает сперматозоиды, и, кроме того, сперма может вытечь из влагалища. Концентрация 60 миллионов сперматозоидов на миллилитр обычно считается нижним пределом для фертильной спермы. Сперма коагулирует сразу после эякуляции, а затем разжижается под действием протеолитических ферментов, главным образом из предстательной железы, что приводит к относительно высокой концентрации свободных аминокислот.Женский оргазм быстро втягивает любой материал, отложившийся в матке, в верхнюю шейку шейки матки, облегчая миграцию сперматозоидов к яйцеклетке и удаляя их из враждебной среды влагалища. Излишне говорить, что женский оргазм не всегда может наступить сразу после мужской эякуляции, и коитус не всегда приурочен к овуляции. Следовательно, подвижность сперматозоидов и долголетие — это адаптации, которые могут обеспечить оплодотворение в неподходящий момент. Факторы окружающей среды: Недавно появились сообщения о том, что количество сперматозоидов снижается во всем мире.Было высказано предположение, что аналоги эстрогенов, выбрасываемые в окружающую среду, например гербициды, которые действуют аналогично эстрогенам, могут попадать в воду и снижать количество и качество сперматозоидов. Кроме того, курение, алкоголь, тепло и некоторые лекарства могут повредить сперму. Концентрация сперматозоидов может сильно различаться у разных людей, на нее отрицательно влияют тяжелые эмоциональные стрессы и физические нагрузки, а также может снижаться длительное воздержание, которое увеличивает долю аномальных сперматозоидов.С другой стороны, хорошее питание и хорошее здоровье полезны. |
Аллергия на семенную жидкость
Вопрос:
10.08.2012
12.04.2018
Я видел 22-летнюю женщину с классическими симптомами аллергии на семенную жидкость с местным отеком и жжением, начинающимися через 3-5 минут после контакта (таких симптомов нет, если ее партнер носит презерватив), после чего последовали 2 дня болезненного полового акта.Это началось вскоре через неделю после ее первой встречи с этим партнером, с которым она начала заниматься сексом два месяца назад. У нее был предыдущий партнер в течение 3 лет без таких симптомов. До этого у нее было несколько бессимптомных половых контактов.Я прочитал всю информацию по этой теме на сайте Ask the Expert и в Medline. Пациентка сделала свой собственный «кожный тест», нанеся эякулят на руку и почесав ее стерильной иглой, и результат был положительным (эритема, отек и зуд)!
Мои вопросы:
1.Стоит ли мне проверить ее? Должен ли я дать образцу разжижиться, а затем центрифугировать, или я могу использовать образец без этой подготовки и должен ли я его «стерилизовать фильтрованием», что у меня нет возможности сделать в моем офисе?
2. Следует ли мне проверять ее партнера на ВИЧ, сифилис и гепатит?
3. Означает ли это, что у нее будут проблемы со всеми последующими партнерами?
4. Следует ли мне проверить ее партнера на предмет раздражения?
5. Если результат отрицательный, могу ли я провести другие анализы (сыворотка и т. Д.)..) или я должен предположить, что это ложноотрицательный результат и что белки в образце не присутствуют в достаточной концентрации, чтобы вызвать положительный ответ?
6. Есть ли еще данные о перекрестной реактивности с аллергенами собак?Как всегда, ценю ваш опыт.
Ответ:
Спасибо за ваш запрос.
Как вы знаете из предыдущих ответов на вопросы «Спроси эксперта» об аллергии на семенную жидкость, доктор Джонатан Бернстайн является всемирно признанным экспертом по этому заболеванию. Он опубликовал множество публикаций в этой области, и поэтому я прошу доктора Бернштейна ответить на ваш запрос. Когда мы получим его ответ, мы перешлем его вам.
Еще раз спасибо за ваш запрос.
С уважением,
Фил Либерман, доктор медицины
Мы получили ответ от доктора Ф.Джонатан Бернштейн. Еще раз благодарим вас за ваш запрос и надеемся, что этот ответ будет вам полезен.
С уважением,
Фил Либерман, доктор медицины
Ответ доктора Джонатана Бернстайна:
В ответ на ваши вопросы:
1) Я бы проверил ее с помощью PST на всю семенную жидкость. Для этого необходимо дать эякуляту разжижиться в течение 30 минут и центрифугировать в течение 10 минут, чтобы отделить семенную жидкость от сперматозоидов. Я бы также проверил ее сексуального партнера в качестве отрицательного контроля.Вам не нужно стерилизовать семенную жидкость для укола. Не следует проводить внутрикожное исследование цельной семенной жидкости, так как это вызовет раздражающую реакцию.
2) И пациентка, и ее половой партнер должны пройти обследование на ЗППП.
3) Раньше у нее не было проблем с другими мужчинами. Это переменно. У одних женщин проблемы со всеми мужчинами, у других — только с одним.
4) При локальной гиперчувствительности семенной плазмы кожные пробы не всегда совпадают с серологическими.Я предлагаю пациентам возможность отправить свою сыворотку, сыворотку своего сексуального партнера и 5-дневный объединенный эякулят в нашу лабораторию для тестирования на sIgE для цельной семенной плазмы.
5) Нет дополнительной свежей информации о перекрестной реактивности между аллергенами собак и семенной плазмой. По нашему опыту с нашими пациентами, мы не обнаружили перекрестной реактивности с аллергеном собаки и ПСА.
6) Мы рекомендуем пациентам с локальной гиперчувствительностью семенной плазмы сначала пройти интравагинальное провокационное исследование; Разведите всю семенную жидкость стерильной водой до разведения 1: 100 000 и закапывайте 10 мл объема интравагинально каждые 10-15 минут до разведения 1: 1, чтобы увидеть, облегчает ли это симптомы.Есть сообщения о случаях, когда это может быть эффективным. В противном случае она может быть кандидатом на подкожную десенсибилизацию к соответствующим фракционированным белкам семенной плазмы.
Джонатан Бернштейн, доктор медицины
26.4D: Semen — Medicine LibreTexts
Сперма — это жидкость, вырабатываемая семенными пузырьками.
ЦЕЛЬ ОБУЧЕНИЯ
Описать сперму
Основные выводы
Ключевые точки
- Семенная жидкость смешивается с жидкостями, вырабатываемыми простатой и бульбоуретральными железами.
- Семенная жидкость обеспечивает питание и защиту сперматозоидов во время их прохождения по женским репродуктивным путям.
- Сперма сначала коагулирует во влагалище, а затем разжижается, позволяя сперме двигаться.
Ключевые термины
- семенной пузырек : одна из двух простых трубчатых желез, расположенных за мужским мочевым пузырем, ответственная за выработку примерно шестидесяти процентов жидкости, которая в конечном итоге становится спермой.
- семенная жидкость : сперма — это жидкость, которая способствует выживанию сперматозоидов и обеспечивает среду, через которую они могут двигаться.
- сперма : жидкость, вырабатываемая в мужских репродуктивных органах животного и содержащая репродуктивные клетки.
Сперма — это органическая жидкость, также известная как семенная жидкость, которая может содержать сперматозоиды. Он секретируется гонадами (половыми железами) и может оплодотворять женские яйцеклетки. У человека семенная жидкость, помимо сперматозоидов, содержит несколько компонентов, в том числе ферменты (протеолитические и другие) и фруктозу. Эти элементы способствуют выживанию сперматозоидов и обеспечивают среду для их подвижности.Сперма вырабатывается и берет свое начало из семенных пузырьков, расположенных в тазу. Процесс, в результате которого выделяется сперма, называется эякуляцией.
Производство и секреция семени
В процессе эякуляции сперма проходит через семявыбрасывающие протоки и смешивается с жидкостями из семенных пузырьков, предстательной железы и бульбоуретральных желез с образованием спермы. Семенные пузырьки производят желтоватую вязкую жидкость, богатую фруктозой, аминокислотами и другими веществами, которые составляют около 70% человеческой спермы.Секрет простаты, на который влияет дигидротестостерон, представляет собой беловатую (иногда прозрачную) жидкую жидкость, содержащую протеолитические ферменты, лимонную кислоту, кислую фосфатазу и липиды. Бульбоуретральные железы выделяют прозрачную жидкость для смазывания просвета уретры.
Защита и транспортировка спермы
Клетки Сертоли, которые питают и поддерживают развитие сперматоцитов, выделяют жидкость в семенные канальцы, которая помогает транспортировать сперму к половым протокам. Эффектные протоки содержат кубовидные клетки с микроворсинками и лизосомными гранулами, которые модифицируют семенную жидкость, реабсорбируя некоторую жидкость.Когда сперма попадает в придаток яичка, основные клетки (которые содержат пиноцитотические сосуды, указывающие на реабсорбцию жидкости) секретируют глицерофосфохолин, который, скорее всего, препятствует преждевременной емкостности.
Семенная плазма обеспечивает питательную и защитную среду для сперматозоидов во время их путешествия по женским репродуктивным путям. Нормальная среда влагалища является враждебной для сперматозоидов, поскольку она кислая (из естественной микрофлоры, вырабатывающей молочную кислоту), вязкая и патрулируется иммунными клетками.Компоненты семенной плазмы пытаются компенсировать эту враждебную среду. Основные амины, такие как путресцин, спермин, спермидин и кадаверин, отвечают за запах и вкус спермы. Эти щелочные основания противодействуют кислой среде влагалищного канала и защищают ДНК внутри сперматозоидов от кислой денатурации.
Характеристики эякулята
По данным Всемирной организации здравоохранения, нормальная человеческая сперма имеет объем 2 мл или больше, pH 7.От 2 до 8,0, концентрация сперматозоидов 20 × 106 сперматозоидов / мл или более, количество сперматозоидов 40 × 106 сперматозоидов на эякулят или более и подвижность 50% или более в течение 60 минут после эякуляции. После эякуляции последняя часть спермы сразу же сворачивается, образуя шарики. Примерно через 15–30 минут простатоспецифический антиген, присутствующий в сперме, вызывает декагуляцию семенного сгустка. Предполагается, что первоначальное свертывание помогает удерживать сперму во влагалище, в то время как разжижение освобождает сперматозоиды, чтобы они могли отправиться в яйцеклетку.