| Бинавит | Р-р д/в/м введения: амп. 2 мл 5, 10 или 20 шт. рег. №: ЛП-000604 от 21.09.11 Дата перерегистрации: 12.07.18 | |||
| Бинавит форте | Таб. | |||
| Битригам | Р-р д/в/м введения: 2 мл амп. 5 или 10 шт. рег. №: ЛП-006421 от 24.08.20 | |||
| Витаксон | Р-р д/в/м введения: 2 мл амп. | |||
| Димексид | Гель д/наружн. прим. 25%: туба 30 г рег. №: ЛП-000501 от 01.03.11 Дата перерегистрации: 07.04.16 | |||
| Дифенин | Таб. | |||
| Дифенин | Таб. 117 мг: 10, 20, 30 или 50 шт. рег. №: ЛП-003509 от 16.03.16 | |||
Таб. | ||||
| Зептол | Таб. 200 мг: 100 шт. рег. №: П N011348/01 от 05.09.11 | |||
| Зептол | Таб. Таб. пролонгир. действия, покр. пленочной оболочкой, 400 мг: 30 шт. рег. №: П N011348/02 от 11.04.12 | |||
| Карбамазепин | ||||
| Карбамазепин | Таб. | |||
| Карбамазепин | Таб. 200 мг: 10, 50 или 100 шт. рег. №: ЛС-001546 от 24.02.11 | |||
| Карбамазепин | Таб. | |||
| Карбамазепин | Таб. 200 мг: 20, 30, 40, 50 или 60 шт. рег. №: ЛП-004756 от 27.03.18 | |||
| Карбамазепин | Таб. | |||
| Карбамазепин | Таб. 200 мг: 50 или 100 шт. рег. №: Р N003681/01 от 05.06.09 | |||
| Карбамазепин Авексима | Таб. | |||
| Карбамазепин ретард-Акрихин | Таб. пролонгир. действия 200 мг: 10, 20, 30, 50 или 100 шт. рег. №: Р N003829/01 от 10.12.09 | |||
| Карбамазепин ретард-Акрихин | Таб. | |||
| Карбамазепин-Акрихин | Таб. 200 мг: 20, 50 или 100 шт. рег. №: Р N000852/01 от 07.09.07 | |||
| Карбамазепин-Ферейн | Таб. | |||
| Комбилипен® табс | Таб., покр. пленочной оболочкой, 100 мг+100 мг+2 мкг: 30 или 60 шт. рег. №: ЛС-002530 от 05.07.10 Дата перерегистрации: 26.12.18 | |||
| КомплигамВ® | Р-р д/в/м введения: амп. | |||
| Мильгамма® | Р-р д/в/м введения 100 мг+100 мг+1 мг+20 мг/2 мл: амп. 5, 10 или 25 шт. рег. №: П N012551/02 от 26.09.11 Дата перерегистрации: 29.06.20 | |||
| Мильгамма® Композитум | Таб. | |||
| Апо-Карбамазепин | Таб. 200 мг: фл. 100 или 500 шт. рег. №: П N011792/01 от 11.08.06 | |||
Дифенина таблетки 0.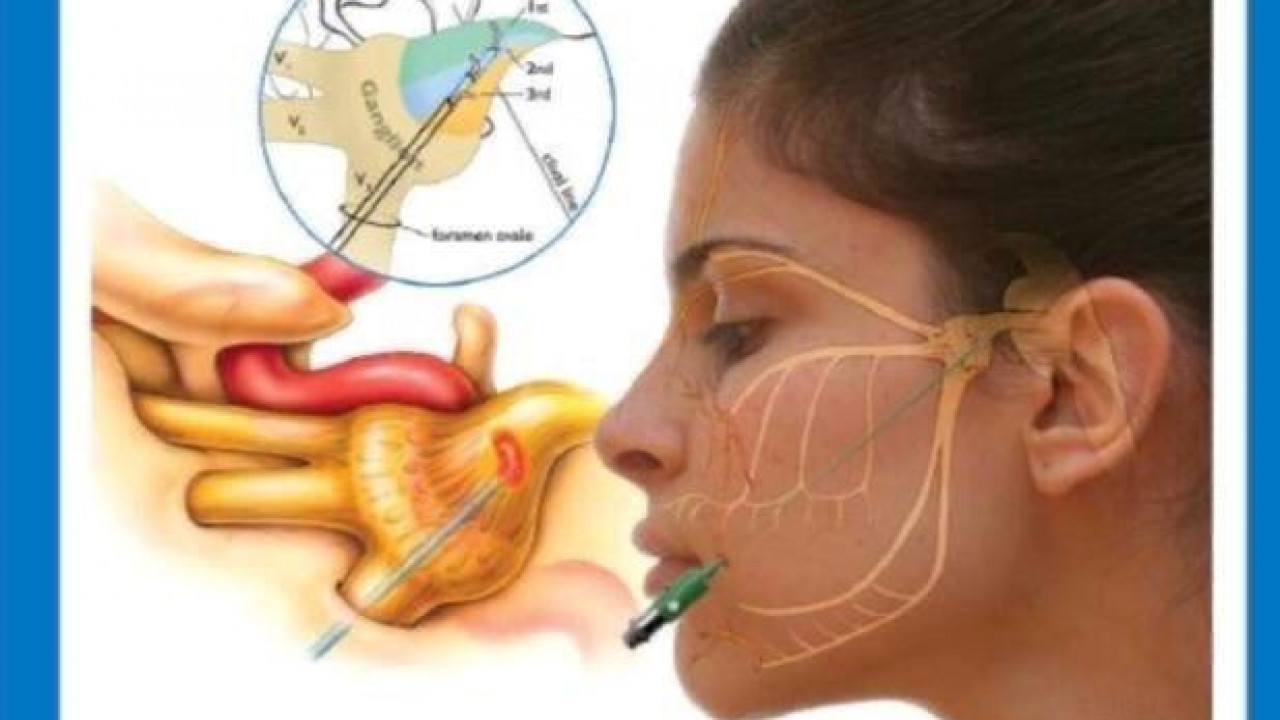 117 г 117 г | Таб. 117 мг: 10, 20, 30 или 50 шт. рег. №: 74/331/63 от 12.04.74 | |||
| Дифенина таблетки 0.117 г | Таб. 117 мг: 10, 20, 30 или 50 шт. рег. №: 74/331/62 от 12.04.74 | |||
Дифенина таблетки 0.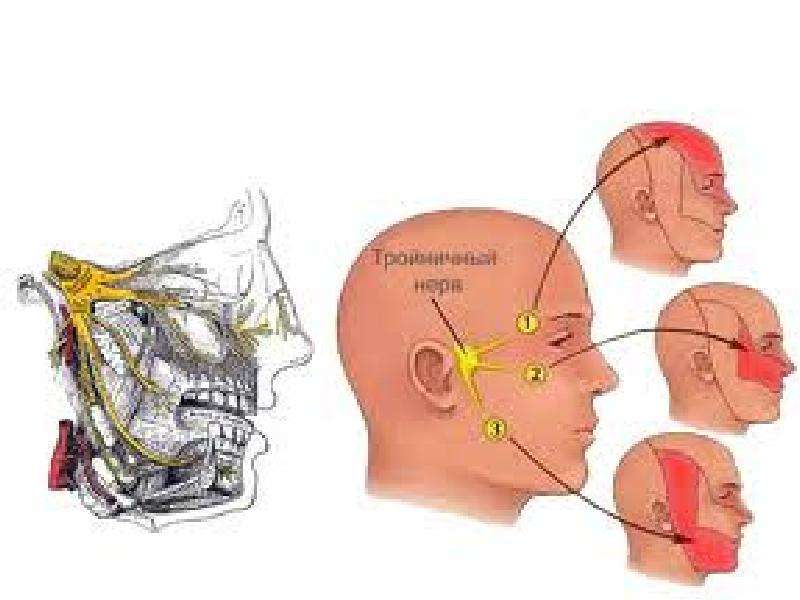 117 г 117 г | Таб. 117 мг: 10, 20, 30 или 50 шт. рег. №: 74/331/63 от 12.04.74 | |||
| Дифенина таблетки 0.117 г | Таб. 117 мг: 10, 20, 30 или 50 шт. рег. №: 74/331/69 от 12.04.74 | |||
| Карбамазепин Никомед | Таб. | |||
| Карбамазепин Никомед | Таб. 200 мг: 50 шт. рег. №: П N012662/01-2001 от 08.02.01 | |||
Карбамазепин таблетки 0. 2 г 2 г | Таб. 200 мг: 50 шт. рег. №: 98/365/4 от 17.12.98 | |||
| Карбамазепин таблетки 0.2 г | Таб. 200 мг: 50 шт. рег. №: 98/365/4 от 17.12.98 | |||
Карбамазепин таблетки 0. 2 г 2 г | Таб. 200 мг: 50 шт. рег. №: 98/365/4 от 17.12.98 | |||
| Карбамазепин таблетки 0.2 г | Таб. 200 мг: 50 шт. рег. №: 98/365/4 от 17.12.98 | |||
Карбамазепин таблетки 0. 2 г 2 г | Таб. 200 мг: 50 шт. рег. №: 98/365/4 от 17.12.98 | |||
| Карбамазепин-Тева | Таб. 200 мг: 20, 30, 50 или 100 шт. рег. №: П N014091/01-2002 от 06.06.02 | |||
| Мазепин | Таб. | |||
Невралгия тройничного нерва | Степанченко А.В.
МГМСУ им. Н.А. Семашко
Невралгия тройничного нерва (НТН) – хроническое рецидивирующее заболевание, протекающее с ремиссиями и обострениями различной продолжительности, отдельные приступы которых проявляются внезапной, интенсивной, стреляющей болью в зонах иннервации 3, 2 и, крайне редко, 1 ветвей тройничного нерва, с преобладанием в правой стороне лица. В европейской медицинской литературе первое описание этого заболевания принадлежит венецианскому врачу Масса (1550 г.), однако в самостоятельную нозологическую форму НТН выделил английский врач Джон Фотергилл (1781 г.) в своей монографии «Болезненные поражения лица». В Международной классификации болезней 10–го пересмотра (МКБ –10) в «поражения тройничного нерва» включаются «невралгия тройничного нерва (синдром пароксизмальной лицевой боли)», «атипичная лицевая боль», «другие поражения тройничного нерва» и «поражения тройничного нерва неуточненные». Международное общество головной боли (МОГБ) в разделе «краниальные невралгии, боли при поражении нервных стволов и деафферентационные боли» рассматривает «тригеминальную невралгию» как «идиопатическую» и «симптоматическую», а также «лицевые боли, не входящие в эту группу».
Взгляды на этиологию и патогенез НТН отличались значительным разнообразием. До начала XX века преобладало мнение о решающей роли в происхождении этого заболевания переохлаждения лица, местных хронических инфекций (зубо–челюстной системы, верхнечелюстных пазух), менингитов и арахноидитов основания мозга. Высказывались мнения о сдавлении периферических ветвей тройничного нерва в узких и длинных каналах лицевого скелета. В качестве причины НТН предполагали нарушения прикуса, необычно высокое стояние верхушки пирамиды височной кости, раздражающее корешок тройничного нерва, кальцификацию арахноидальных оболочек. В настоящее время общепринятой является точка зрения о решающей роли в происхождении НТН сдавления корешка пятого нерва в месте его входа в мозговой мост патологически извитым кровеносным сосудом (обычно передней верхней мозжечковой артерией), опухолями мосто–мозжечкового узла (акустической невриномой, арахноэндотелиомой) или бляшками рассеянного склероза. Полагают, что сдавление патологически извитым кровеносным сосудом встречается в 88%, опухолями мосто–мозжечкового угла в 6% и бляшками рассеянного склероза также в 6%. Патологический механизм возникновения боли наиболее убедительно объясняется теорией «воротного контроля» Мелзака и Уолла (1965 г.). При сдавлении корешка тройничного нерва в зоне его входа в мозговой мост патологически извитой верхней передней мозжечковой артерией (реже другим патологическим образованием) происходит поражение волокон глубокой чувствительности верхне– и нижнечелюстного подразделений из–за особенностей типичных анатомических соотношений чувствительных волокон в этом отделе системы тройничного нерва. В нормальных физиологических условиях стимуляция быстропроводящих нервных волокон глубокой чувствительности тормозит поток сигналов по волокнам поверхностной чувствительности, проводящей болевые сигналы. При нарушении целостности нервных волокон возникает контакт между волокнами глубокой и поверхностной системы, поэтому стимулы в норме вызывающие торможение болевых сигналов (движение нижней челюсти, глотание и др.), напротив, будут способствовать усилению болевого потока в чувствительных ядрах тройничного нерва ствола мозга и запускать типичный сигнал, субъективно ощущаемый в виде боли. Разумеется, в оформлении болевого ощущения при приступах невралгии тройничного нерва принимают участие и другие многообразные стволовые, подкорковые и корковые структуры, но вышеописанный механизм возникновения боли, по–видимому, является ведущим.
По данным многолетних наблюдений клиники нервных болезней стоматологического факультета Московского государственного медико–стоматологического университета, невралгией тройничного нерва женщины заболевают чаще мужчин в соотношении 3:1, правосторонняя локализация встречается в 70% , левосторонняя в 29%, а двусторонняя – в 1%. Средний возраст, поступающих больных НТН в клинику впервые составляет 55 лет, тогда как анамнестические данные свидетельствуют о начале заболевания на 8–10 лет раньше. Первый приступ боли без всякой видимой причины наступает в 34%, совпадает с лечением зубов в 27%, с отрицательными эмоциями – у 17%, у остальных началу заболевания сопутствуют самые различные факторы (внезапное переохлаждение лица, респираторная инфекция, локальные травмы и др.).
Только у 23% больных НТН дебютирует развернутым болевым синдромом, тогда как у остальных – ограниченными, локальными, малоинтенсивными, стреляющими, дергающими или прокалывающими болями в области альвеолярного отростка или медиальных отделах лица. Такие приступы боли возникали по несколько раз в день, без четкой связи с запускающими факторами или зонами. Разнообразные виды амбулаторной терапии (акупунктура, парантеральная витаминотерапия, физиотерапия), приводили к прекращению болевого синдрома в среднем на 18 месяцев. У некоторых пациентов регресс таких умеренных болевых проявлений происходил и без всякого лечения.
Развернутый типичный болевой пароксизм невралгии тройничного нерва достаточно характерен и состоит из нескольких ключевых симптомов:
1. Кратковременная, никогда не превышающая двух минут (в среднем 10 – 12 секунд) чрезвычайно интенсивная боль стреляющего характера, сравниваемая больными с ударом электрического тока.
2. Между отдельными приступами боли имеется «светлый промежуток», разной продолжительности, в зависимости от характера обострения.
3. Рисунок боли всегда имеет определенную протяженность в границах сегментарной иннервации тройничного нерва и существенно не изменяется при последующих обострениях.
4. Наличие пусковых зон – гиперчувствительных участков на коже лица (обычно в области носогубного треугольника) и в полости рта, слабое раздражение которых приводит к типичному болевому приступу.
5. Наличие запускающих факторов – действий или условий, при которых возникают типичные присупы боли при НТН. Чаще всего это умывание, жевание, глотание, разговор, иногда даже дуновение ветра.
6. Типичное болевое поведение. Как правило, во время приступа боли больные не плачут, не кричат, а замирают в одной позе, в которой их застает приступ и, стараясь не двигаться, пережидают болевой период. Иногда растирают зону боли или давят на нее.
7. Избегание раздражения пусковой зоны. Когда больного просят указать ее, он не доносит палец на несколько сантиметров до гиперчувствительного участка, опасаясь спровоцировать приступ боли, а когда врач пытается коснуться этого участка, непроизвольно отшатывается.
8. На высоте болевого приступа могут возникнуть подергивания лицевой мускулатуры, однако в последнее время, в связи с применением для лечения НТН противоэпилептическими препаратами, этот симптом встречается редко.
9. Отсутствие чувствительного дефицита в зоне боли. Исключение при этом составляют больные после хирургических методов лечения НТН.
Традиционно описываемая болезненность точек выхода ветвей тройничного нерва на лицо (супраорбитальная вырезка, подглазничное и подбородочное отверстие) существенного диагностического значения не имеют, а возникающий при этом болевой приступ связан со стимуляцией пусковых зон соответствующего участка лица.
Первый визит при дебюте НТН, как правило, происходит к стоматологу, так как гиперчувствительные зоны у подавляющего числа больных располагаются не только на лице, но и в полости рта. До конца XX века, когда стоматологи были в меньшей степени знакомы с этиологией НТН, на стороне болевых приступов нередко ошибочно удалялись здоровые зубы. Следует, впрочем, заметить, что удаление зубов производилось по настоятельному требованию самих больных, связанному с тем, что после очередного удаления зуба болевые пароксизмы на некоторое время прекращались. Такое явление можно объяснить с позиций теории «ворот боли», когда раздражение рецепторов глубокой чувствительности околозубных тканей приводит к выделению тормозных медиаторов в стволовом ядерном комплексе тройничного нерва и временному прекращению приступов невралгии.
В период ремиссий сохраняется фобический синдром, с формированием охранительного поведения, т.к. больные, опасаясь наступления рецидива заболевания, всегда едят на половине рта противоположной боли и укутывают голову даже в теплую погоду.
Стадия развернутых болевых приступов может продолжаться десятки лет с ремиссиями и обострениями, но со временем, в старческом возрасте типичные невралгические приступы боли приобретают невропатические черты в виде легких болей, уменьшения интенсивности острой боли возникновения тупой постоянной атипичной лицевой боли.
По–видимому, определенная стадийность в течении НТН объясняется особенностями поражения корешка тройничного нерва под влиянием сдавления патологическими образованиями мосто–мозжечкового угла.
Следует иметь в виду, что при стойком болевом синдроме, появлении симптомов неврологического дефицита как со стороны тройничного, так и других черепных нервов (особенно лицевого и слухового), следует проводить тщательное обследование структур задней черепной ямки (МРТ, слуховые вызванные потенциалы и др.) для выявления возможного объемного образования и неотложного нейрохирургического вмешательства.
В классификационных критериях МАИБ, МОГБ имеются описательные характеристики атипичных болевых синдромов лицевого нерва, близких по клиническим проявлениям НТН. Важнейшими среди них являются следующие:
Вторичной НТН при лицевой травме присуща хроническая, пульсирующая, жгучая боль с пароксизмальными усиливающимися приступами в зонах распределения конечных ветвей тройничного нерва. Болевой синдром отличается умеренностью, продолжительностью, со временем присоединяются незначительные трофические нарушения. Хронологически начало заболевания совпадает с травмой лица, реконструктивными операциями или затрудненным удалением зубов.
SUNCT – синдром (англ. аббревиатура слов – кратковременная, односторонняя, невралгоподобная боль с конъюнктивитом и слезотечением). Проявляется односторонними, длящимися десятки секунд, обычно дневными периорбитальными болями, сопровождающимися преходящим конъюнктивитом, слезотечением и потением лба. Неврологического дефицита нет.
Единственным эффективным препаратом для консервативного лечения НТН является карбамазепин (Тегретол и др.). Карбамазепин, синтезированный Шиндлером в 1957 г. и введенный в клиническую практику терапии НТН Блумом в 1963 г., представляет по своим химическим свойством призводное иминостильбена, способность которого уменьшать проницаемость мембран нейронов, участвующих в ноцицептивных реакциях, для натрия и обусловливает его противоболевое действие.
Тегретол оказывает противосудорожный и одновременно психотропный эффект. Его можно назначать как основное лечебное средство, так и в сочетании с другими противоэпилептическими препаратами. Психотропный эффект Тегретола способствует повышению коммуникабельности больных и их социальной реабилитации. При эссенцальной невралгии тройничного нерва Тегретол в большинстве случаев предупреждает появление пароксизмальных болей. Тегретол вызывает быстрое улучшение при психических и вегетативных симптомах.
Тегретол – противоэпилептический препарат, с периодом полураспада 20–40 часов (при повторных приемах и комбинированной терапии с другими противосудорожными препаратами он может снижаться до 8–12 часов), достаточно полно, но медленно и неравномерно всасывается из стандартных таблеток в верхнем и нижнем отделах кишечного тракта, с достижением максимального уровня содержания в сыворотке крови через 4 – 8 часов. Активное вещество карбамазепин соединяется с белками плазмы (около 75%), почти полностью метаболизируется в печени и переходит в активный метаболит – эпоксид, также обладающий противосудорожными свойствами.
Противопоказаниями к этому препарату являются заболевания костного мозга, предсердно–желудочковая блокада, гипонатриемия, комбинирование с ингибиторами моноаминооксидазы, препаратами лития, малые эпилептические припадки. Эффективность действия карбамазепина повышают дилтиазем, верапамил, никотинамид, эритромицин, а снижают вальпроаты, галоперидол, фенобарбитал. Препарат выпускается в виде таблеток 200 и 400 мг, таблеток с пролонгированным действием с разделительной бороздкой по 200 и 400 мг, разжевываемых таблеток по 100 мг и в виде сиропа (2%) (флаконы по 100 и 250 мл).
При НТН обычно назначается следующая схема лечения:
– два дня по 100 мг 3 раза в сутки (суточная доза 300 мг), – два дня по 200 мг 2 раза в сутки (суточная доза 400 мг), – два дня по 200 мг 3 раза в сутки (суточная доза 600 мг), – три дня по 200 мг 4 раза в сутки (суточная доза 800 мг).
При отсутствии противоболевого эффекта переходят к более высоким дозировкам – 1000 и 1200 мг в сутки, с распределением на 4–6 приемов. Рекомендуемая начальная доза для пациентов пожилого возраста составляет по 100 мг 2 раза/сут. При достижении достаточно выраженного результата следует остановиться на соответствующей суточной дозе в течение месяца и затем также медленно снизить эффективную дозу. Лечение карбамазепином на таком количестве необходимо продолжать без перерыва не менее, чем полгода, а затем перевести на поддерживающие дозы (200–400 мг в сутки в два приема). В последнее время карбамазепин (Тегретол) производится в сиропе, что хорошо переносится больными НТН.
Таблетки и сироп Тегретола следует принимать вместе с едой или после еды с небольшим количеством жидкости. Сироп следует взбалтывать до употребления. Разжевываемые таблетки следует принимать после еды с небольшим количеством жидкости. Таблетки с пролонгированным действием (или целиком или, если так выписано, только половину) проглатывать вместе с едой или после еды с небольшим количеством жидкости, не разжевывая их. Разжевываемые таблетки и сироп особенно годятся для пациентов, которые с трудом проглатывают таблетки. Благодаря медленному, контролированному высвобождению активного вещества из таблеток, имеющих бороздку для деления, суточную дозу можно, как правило, принимать в 2 приема. Перед началом лечения необходимо провести исследование функции печени и картины крови. Впоследствии анализ крови следует проводить в течение первого месяца лечения еженедельно, а затем ежемесячно. Контроль функции печени должен осуществляться периодически. Непрогрессирующая или устойчивая асимптоматическая лейкопения, которая часто наблюдается, в общем не требует отмены препарата. Однако лечение Тегретолом следует прекратить при появлении прогрессирующей лейкопении или лейкопении, сопровождающейся клиническими симптомами, такими как лихорадка или ангина. Препарат обладает хорошей переносимостью. В отдельных случаях, особенно в начале лечения, могут наблюдаться такие побочные действия, как потеря аппетита, сухость во рту, рвота, диарея, запор, головная боль, головокружение, сонливость, атаксия, нарушения аккомодации, диплопия, у пожилых людей может наблюдаться спутанность сознания и возбуждение. Эти побочные явления, как правило, исчезают через 7–14 дней сами собой или после временного уменьшения дозы Тегретола.
Менее эффективным препаратом, чем карбамазепин, но все же обладающим достаточно выраженнным противоболевым действием, является фенитоин. Фенитоин назначается 2–3 табл в сутки, противопоказания – нарушения функций печени и почек, кахексия, нарушения сердечного ритма, порфирия. Среди побочных реакций наиболее часто встречаются ажитация, вертиго, гиперплазия десен, контрактура Дипюитрена и др. Эффективность этого препарата повышают пропанолол, хлордиазепоксид, а снижают – стероиды, фолиевая кислота, галоперидол.
У ряда больных НТН противоболевое действие оказывают некоторые другие препараты, ряд убывающей эффективности которых представлен следующим образом – карбамазепин, фенитоин, клоназепам, вальпроевая кислота.
В период обострения НТН используется внутривенное (более эффективно капельное) введение натрия оксибутирата, по 5 мл 20 % раствора дважды в сутки (противопоказанием является гипокалемия), внутривенное струйное введение никотиновой кислоты 1%, начиная с 1 мл, с постепенным повышением до эффекта «воспламенения» (обычно 6–8 мл) и снижением к исходной дозе.
В период обострения применяется ультрафонофорез гидрокортизона, лазеропунктура на болевые точки, классическая акупунктура.
При сопутствующих спастических состояниях, сопровождающихся болевым синдромом при НТН, используются антиспастические препараты – миорелаксанты. Одним из представителей этой группы является тизанидин (Сирдалуд). Сирдалуд – миорелаксант центрального действия. Стимулируя пресинаптические a2–адренорецепторы, он приводит к угнетению полисинаптической передачи возбуждения в спинном мозге, вызывающей мышечный гипертонус. Препарат эффективен при болях умеренной или высокой интенсивности, особенно когда боль усиливается в течение ночи. Препарат характеризуется хорошей переносимостью. Доза подбирается индивидуально в течение 2–4 нед. и составляет 2–6 мг/сут.
При неэффективности консервативной терапии альтерантивым методов являются нейрохирургические методы лечения – ретрогассеральная терморизотомия, микроваскулярная декомпрессия тригеминального корешка и др
.
Симптомы и причины возникновения невралгии. Чем лечить невралгию.
Что такое невралгия?
Невралгиями называют поражения периферических нервов. Симптомы невралгии — приступы боли в зоне, так называемой иннервации, то есть в тех участках, где орган или ткань окружены нервами для связи с центральной нервной системой. Невралгия может возникнуть в любой части тела и имеет различные причины.
Причины возникновения невралгии
Среди наиболее частых причин невралгии – переохлаждение, инфекционные заболевания, тяжелое течение острых респираторных вирусных инфекций, травмы, воспаления и опухоли. Распространенными являются невралгия тройничного нерва и межреберная невралгия. При поражении тройничного нерва боль локализуется в области лица. Человек страдает от приступов, которые могут быть вызваны как легкими прикосновениями (например, к щеке или носу), так и холодной или горячей пищей, чисткой зубов, вспышкой света или громким звуком. Само поражение нерва вызвано, как правило, травмой лица, воспалительными процессами в пазухах носа или нелеченых зубах. Профилактика невралгии возможна лишь в тех случаях, когда речь идет о запущенных воспалительных процессах, так как на развитие опухолей или возникновение инфекционных заболеваний мы влиять не можем.
Невралгия тройничного нерва чаще всего возникает у женщин, причем в зрелом возрасте.
Причиной межреберной невралгии (торакалгии) обычно является остеохондроз позвоночника, преимущественно грудного отдела. Резкая боль в области ребер может возникать при глубоком вдохе, чихании или кашле. Кроме того, возможно развитие межреберной невралгии на фоне сердечно-сосудистых заболеваний, связанных с недостаточным притоком кислорода к нервам.
Уменьшить вероятность новых приступов невралгии помогает выполнение простых правил: нужно избегать стрессов, больше спать, соблюдать умеренность в употреблении алкоголя, ограничить физические нагрузки, а также своевременно лечить воспалительные и инфекционные заболевания.
Существуют и другие локализации невралгии: в бедре, крылонебном узле (вызывает боль в шее, небе, висках, глазах), в затылке (при этом боль распространяется в области глаз, затылка, висков, усиливается во время движений головой и может сопровождаться рвотой). Во всех случаях невралгия может быть вызвана как переохлаждением или травмой, так и быть следствием хронического заболевания. Симптомы такой болезни, как невралгия, требуют подтверждения у врача, так как могут «маскироваться» под другие заболевания.
Как и чем лечить невралгию, и возможно ли лечение невралгии в домашних условиях
Если невралгия связана с ранее возникшим заболеванием, его необходимо лечить, чтобы избежать дальнейшего поражения периферических нервов и начать восстановительные процессы.
В любом случае лечение невралгии предполагает прием препаратов, уменьшающих боль. При лечении невралгии назначают такие препараты:
- инъекции обезболивающих препаратов (местно)
- миорелаксанты (препараты для расслабления мышц)
- нестероидные противовоспалительные препараты
- гормональные препараты
- витамины группы В
Хороших результатов в лечении невралгий позволяет достичь физиотерапия, в том числе с использованием ультразвука, инфракрасных и ультрафиолетовых лучей, лазера, иглоукалывания и других методик. В крайних случаях применяют хирургическое лечение.
Витамины группы B при лечении невралгии
Витамины группы B принимают участие во многих метаболических процессах, в том числе, непосредственно затрагивающих нервную систему. Они отвечают за передачу нервных импульсов, обмен в тканях нервной системы, восстановление нервов после поражений или травм. Среди наиболее важных нейротропных витаминов — B1 и B6 (бенфотиамин и пиридоксин), содержащиеся в дозе по 100 мг в препарате Мильгамма® таблетки. Противовоспалительный, обезболивающий, восстановительный эффекты бенфотиамина и пиридоксина способствуют быстрому выздоровлению, значительно улучшают качество жизни благодаря эффективному воздействию на болевой синдром. Однако не следует лечить невралгии самостоятельно, полагаясь только на витамины. Прежде всего, нужна точная диагностика, которая поможет определить причину невралгии. Далее врач прописывает комплексное лечение, которое иногда может включать гормональные препараты при невралгии и другие медикаментозные средства, которые нельзя принимать без назначения специалистом. При этом применение препарата, содержащего витамины группы B – это действительно необходимость, если речь идет о лечении болевого синдрома, связанного с поражениями нервов.
Профилактика невралгии при хроническом течении заболевания
К сожалению, да, если не выявить причину поражения периферических нервов и не устранить ее. Если невралгия первичная, то есть, возникла в результате, например, переохлаждения или травмы, важно пройти полный курс лечения, чтобы не допустить развития хронического процесса. Боль при невралгиях может быть очень сильной, что значительно ухудшает качество жизни и снижает трудоспособность, поэтому полноценное лечение необходимо. Не стоит забывать и о том, что состояние нашей нервной системы зависит от уровня стресса, в котором находится организм, и боль иногда может усиливаться по психосоматическим причинам, то есть, буквально зависеть от наших мыслей.К сожалению, да, если не выявить причину поражения периферических нервов и не устранить ее. Если невралгия первичная, то есть, возникла в результате, например, переохлаждения или травмы, важно пройти полный курс лечения, чтобы не допустить развития хронического процесса. Боль при невралгиях может быть очень сильной, что значительно ухудшает качество жизни и снижает трудоспособность, поэтому полноценное лечение необходимо. Не стоит забывать и о том, что состояние нашей нервной системы зависит от уровня стресса, в котором находится организм, и боль иногда может усиливаться по психосоматическим причинам, то есть, буквально зависеть от наших мыслей.
Что такое невралгия?
Невралгия (от др.-греч. νεῦρον — «жила, нерв» + ἄλγος — «боль») — это поражение периферических нервов. Невралгия характеризуется острой, ноющей, жгучей или тупой болью по ходу нерва, возникающей приступами. Причины могут быть разными, среди них: заболевания самого нерва и нервных сплетений, результат травм и инфекций, резкое переохлаждение, воспаления и опухоли, хронические расстройства, заболевания позвоночника и т. п. Приступ может возникнуть в любой части тела, но наиболее часто встречаются невралгии тройничного, затылочного и межреберных нервов.
При поражении тройничного нерва боль концентрируется в области лица. Неприятные ощущения могут быть вызваны легкими прикосновениями, холодной или горячей пищей, чисткой зубов, а также вспышкой света или громким звуком. Сигналом о начале приступа могут послужить зуд или мурашки, а после появляется резкая боль, продолжающаяся несколько минут. Подобное поражение обычно происходит вследствие травмы лица, воспалительных процессов в пазухах носа или заболеваний зубов (в том числе неправильного прикуса). Невралгия тройничного нерва чаще всего возникает у женщин в зрелом возрасте.
Межреберная невралгия (или торакалгия) — это остеохондроз позвоночника, преимущественно грудного отдела. Такой тип проявляется резкой болью в области ребер, которая может возникнуть при глубоком вдохе, чихании, смехе или кашле. Развитие межреберной невралгии нередко наблюдается на фоне сердечно-сосудистых заболеваний, которые связаны с недостаточным притоком кислорода к нервам.
Основным признаком невралгии затылочного нерва является нестерпимая, пульсирующая боль в голове (от затылка к вискам, а также в области глаз), усиливающаяся при движении головой. Приступ может даже сопровождаться рвотой.
Существуют и другие виды невралгии. Стреляющая боль на наружной поверхности бедра — это невралгия наружного кожного нерва бедра. Симптомы усиливаются при движении, сопровождаясь при этом ощущается жжение и онемение на коже.
Особенно тяжело проявляется невралгия крылонебного узла. Приступ начинается неожиданно, обычно ночью, и может продолжаться от нескольких часов до двух дней. Жгучая боль охватывает нёбо, виски, область глаз, шею, а далее распространяется по рукам.
Самым редким типом является невралгия языкоглоточного нерва. Она характеризуется болями в глотке, которые распространяются на ухо и нижнюю челюсть.
Симптомы невралгии требуют подтверждения у врача, так как нередко могут маскироваться под другие заболевания.
Снизить вероятность возникновения невралгии возможно. Для этого нужно следовать нескольким простым правилам: избегать стрессов, не пренебрегать сном, умеренно употреблять алкоголь и не перегружать тело физическими нагрузками, а также своевременно лечить воспалительные и инфекционные заболевания.
Как и чем лечить невралгию?
Когда невралгия связана с ранее возникшим заболеванием, необходимо в первую очередь лечить именно его. Это позволит избежать дальнейшего поражения периферических нервов. Если невралгия первичная (является результатом переохлаждения или травмы), важно пройти полный курс комплексной терапии, чтобы не допустить развития хронического процесса.
Боль при невралгиях нередко бывает настолько сильной, что значительно сказывается на качестве жизни, снижая трудоспособность человека. Поэтому необходимо прибегать к помощи обезболивающих препаратов. Для снятия симптомов применяются нестероидные противовоспалительные препараты быстрого направленного действия (таблетки, гели). Также могут назначаться инъекции обезболивающих средств (местно), миорелаксанты (для расслабления мышц), гормональные препараты и витамины группы В.
Высокие результаты в лечении невралгий достигаются с помощью физиотерапии, в том числе с использованием ультразвука, иглоукалывания и других терапевтических методик. В особенно серьезных случаях необходимо хирургическое вмешательство.
Профилактика невралгии возможна только при запущенных воспалительных процессах, когда предсказать или повлиять на причины возникновения невралгии мы не можем.
Важно помнить и о том, что состояние нашей нервной системы зависит от уровня стресса, в котором находится организм. Так, интенсивность болей может носить психосоматический характер, другими словами — зависеть от наших мыслей.
Источники:
https://info.wikireading.ru/73948
https://milgamma.com.ua/ru/nevralgia/
https://medportal.ru/enc/neurology/nevralgia/nevralgia/
Таблетки, инъекции, мази при лицевом неврите
- Высокие результаты, отсутствие побочных эффектов
- Лечение без таблеток и операций
- Первичная консультация врача БЕСПЛАТНО
Записаться
Неврит лицевого нерва – это воспалительное заболевание, которое проявляется нарушением чувствительности, мышечных сокращений (двигательной активности) в области лица. Чтобы уменьшить эти симптомы врач назначает комплекс препаратов, включая противовоспалительные и мышечные средства.
Болевые проявления нетипичны для лицевого неврита, потому обезболивающие препараты (анальгетики, анестетики) при этом заболевании, как правило, не требуются.
- Нестероидные противовоспалительные препараты (НПВП) назначаются в виде таблеток или мазей. Уменьшают воспаление нерва, облегчают боль в области уха, лица. Уменьшают отечность мягких тканей, сдавление нерва.
- Стероидные (гормональные препараты) применяются в случаях, когда негормональные средства не дают достаточного противоотечного, противовоспалительного эффекта. Наряду со снятием воспаления улучшают прохождение нервных импульсов и иннервацию лицевых мышц, препятствуют развитию мышечных контрактур. Оказывают мощное действие, но показаны для однократного или редкого (ситуативного) применения из-за высокой вероятности побочных эффектов и привыкания. Обычно применяются в виде таблеток или инъекций.
- Мочегонные препараты назначаются, чтобы уменьшить отечность, вывести межклеточную жидкость из мышечных тканей и тем самым уменьшить давление на сдавленный нерв. Назначаются в виде таблеток.
- Спазмолитики уменьшают мышечное напряжение, облегчают спазмы, улучшают сократительную активность лицевых мышц, помогают восстановлению мимики. Уменьшают спазмы кровеносных сосудов, улучшают кровообращение, кровоснабжение и питание лицевого нерва, активизируют обменные процессы. Оказывают косвенное обезболивающее, противовоспалительное действие. Назначаются в виде таблеток.
- Нейротропные препараты улучшают проводимость нервных волокон, помогают устранить непроизвольные сокращения мимических мышц (тики), улучшают прохождение нервных команд к мышцам и сигналов от чувствительных рецепторов, оказывают укрепляющее действие на нервные ткани.
- Витамины В1, В6, В12 оказывают укрепляющее действие на нервную систему, в том числе лицевой нерв, улучшают работу нейронов, позитивно влияют на межнейронные связи. Назначаются в виде таблеток.
- Противовирусные препараты назначаются при инфекционных формах лицевого неврита, подавляют вирус герпеса. Назначаются в виде таблеток.
- Антихолинэстеразные препараты увеличивают концентрацию нейромедиатора ацетилхолина в межнейронных связях, благодаря этому улучшают прохождение нервных сигналов, иннервацию и работу лицевых мышц, слюнных, слезных желез.
Немедикаментозные средства
Методы восточной медицины, применяемые в клинике «Тибет», не уступают в эффективности фармацевтическим препаратам, но при этом не вызывают привыкания и не дают побочных эффектов.
- Иглоукалывание оказывает спазмолитическое, противоишемическое, антивоспалительное, обезболивающее действие. Уменьшает отечность, воспаление, снимает боль. Повышает выработку ацетилхолина, дофамина и других нейромедиаторов, улучшает проводимость нервных волокон и прохождение нервных сигналов.
С помощью акупунктуры врач устраняет перекос, парез, онемение лица, восстанавливает иннервацию мимических мышц, слюнных и слезных желез, нормализует чувствительность лица.
- Точечный массаж лица снимает мышечные спазмы, улучшает кровообращение, приток крови к лицевому нерву и его питание, устраняет застойные явления, скопление межклеточной жидкости и отечность мягких тканей, активизирует обменные процессы, стимулирует восстановительные, защитные механизмы, работу иммунной системы.
- Фитопрепараты тибетской медицины снимают воспаление, улучшают работу кровеносных сосудов, повышают эластичность и сократительную активность сосудистой стенки, позитивно влияют на нервную систему, помогают устранить последствия стрессов, повысить устойчивость к холоду, стрессовым нагрузкам. Повышают иммунитет, оказывают противовирусное и ангиопротекторное действие. Закрепляют результаты лечебных процедур.
Бесплатная консультация Опрос, осмотр, пульсовая диагностика от 30 минут
Диагностика УЗИ, МРТ, Лабораторные исследования (по назначению)
Лечение Индивидуальный
план
Кто занимается лечением
данного заболевания
Невралгия тройничного нерва — современные методы лечения
Лечение невралгии тройничного нерва обычно начинается с назначения медицинских препаратов, подавляющих боль и многим людям этого достаточно длительное время. Однако, со временем, у части пациентов развивается привыкание к медикаментам, что проявляется снижением их эффективности, вплоть до полной потери эффекта. Также нередки случаи развития существенных нежелательных побочных эффектов. Для подобных случаев существуют более радикальные методики лечения.
Если же причиной болей в лице являются другие заболевания, то также необходимо лечение, направленное на основную причину.
Общепринятым мировым подходом является начало лечения с медикаментозной терапии с последующим проведением (при необходимости) реконструктивных вмешательств (микрососудистой декомпрессии корешка тройничного нерва), а при невозможности ее проведения или же неэффективности выполняются деструктивные (разрушающие нерв) вмешательства.
Медицинские препаратыДля лечения тригеминальной невралгии тройничного нерва Вам могут назначить лекарства, которые уменьшают или прекращают передачу болезненных сигналов, посылаемых в Ваш мозгимпульсов.
- Антиконвульсанты. Обычно назначают карбамазепин (финлепсин), эффективность которого при лечении тригеминальной невралгии тройничного нерва подтверждена. Другой Другие антиконвульсанты, который которые может могут применяться при данном состоянии – — это окскарбазепин (Трилептал), ламотриджин (Ламиктал) и топироматы (Топиромакс). Также могут применяться препараты других групп, такие как клоназепам, габапентин, прегабалин. Если препараты, которые Вы принимаете теряют свою эффективность, может потребоваться корректировка дозы или смена препарата, которую необходимо производить под контролем лечащего врача. Побочные эффекты могут включать в себя головокружение, заторможенность, сонливость, двоение в глазах и тошноту. Во время приема препаратов следует воздержаться от управления автомобилем и работы с механизмами, которая требует повышенного внимания или травмоопасна.
- СпазмолитикиМышечные релаксанты. Препараты с мышечно-расслабляющим действием, такие как баклофен (Габлофен, Лиоресал) могут применяться самостоятельно или в комбинации с карбамазепином.
- Антидепрессанты. В многие протоколы лечения хронических болевых синдромов входят препарат группы антидепрессантов (Амитриптилин, Флуоксетин (Прозак), Пароксетин)), которые показали свою эффективность при правильном применении.
При невралгии тройничного нерва, цель хирурга – — прекратить сдавление и раздражение тройничного нерва прилежащим сосудом или же, в ряде случаев, разрушить его волокна, для прерывания прекращения патологического функционирования. Разрушение нерва приводит к онемению лица на стороне вмешательства, которое в зависимости от процедуры и особенностей заболевания, может сохраниться быть постояннопостоянным. После любого хирургического вмешательства боль может возобновиться спустя несколько месяцев или лет. Частота рецидивов зависит от типа невралгии и характера проведенного вмешательства.
Варианты хирургических операций при тригеминальной невралгии (оперативное лечение невралгии тройничного нерва) включают:Микрососудистая декомпрессия. «Золотой стандарт» хирургического лечения невралгии тройничного нерва. Эффективность вмешательства составляет 96-97,5%, что также делает ее одной из самых эффективных операций в плановой нейрохирургии. Операция относится к реконструктивному типу вмешательств, что означает максимальное сохранение анатомических структур и их нормальных функций.
Процедура заключается в отведении сосуда от тройничного нерва в зоне их контакта.
Во время операции хирург делает разрез позади уха на стороне боли. Затем через небольшое отверстие в черепе, хирург отводит все сосуды от нерва, которые находятся с ним в контакте и изолирует их друг от друга специальной прокладкой. Если нерв сдавливается веной, хирург может ее удалить. Также врач может пересечь часть волокон нерва (нейротомия) во время операции, в зависимости от особенностей анатомических взаимоотношений и характера сосудисто-нервного конфликта.
В подавляющем большинстве случаев микрососудистая декомпрессия приводит к полному прекращению боли или значительному ее уменьшению. Данное вмешательство, как и все хирургические операции несет определенные риски, которые включают малый в небольшом проценте случаев снижения снижение слуха, слабости слабость мышц лица, онемение лица, двоение в глазах и другие общехирургические осложнения. Более подробную информацию сообщит Ваш лечащий врач при личной беседе. Большинство пациентов после этой процедуры не имеют каких-либо стойких неврологических симптомов. Данная процедура имеет наименьший процент возобновления болей в долгосрочной перспективе, в сравнении с другими методиками лечения.
Деструктивные методики хирургического лечения невралгии тройничного нерваОстальные методики хирургического лечения являются деструктивными, то есть предполагают разрушение волокон тройничного нерва или иных структур, вовлеченных в процесс.
- Радиохирургия. При этой процедуре, производится сфокусированное радиационное воздействие на корешок тройничного нерва. Данная техника и спользует радиацию для того чтобы разрушить тройничный нерв и снизить или прекратить передачу по нему болевых импульсов. Эффект наступает постепенно, что может занимать несколько недель. После процедуры развивается онемение половины лица, которое сохраняется длительное время. В случае рецидива и возобновления боли процедуру повторяют.
Несомненный плюс процедуры – — это ее безболезненность и отсутствие необходимости в госпитализации и проведении хирургической операции. Среди минусов – — высокая стоимость, и тот факт, что она не устраняет причину заболевания – — сдавление корешка нерва. Деструктивный характер процедуры, в случае ее неэффективности, значительно снижает или сводит на нет эффективность возможного проведения микрососудистой декомпрессии. Иногда может происходить усиление болей на фоне онемения лица – — так называемая «болезненная анестезия» – — «anesthesia dolorosa»
Другие процедуры, которые могут применяться для лечения тригеминальной невралгии тройничного нерва, называются «ризотомия». При ризотомии, хирург проводит разрушение волокон нерва, что приводит к онемению лица.
Способы ризотомии включают:- Инъекции глицерола (Глицероловые блокады). Во время данной процедуры игла проводится через лицо к отверстию на в основании черепа, через которое затем игла вводится в тригеминальную цистерну, небольшую полость со спинномозговой жидкостью, которая окружает узел тройничного нерва —- место, где нерв делится на три ветви – — и часть его корешка. Затем доктор вводит небольшое количество стерильного глицерола, который повреждает тройничный нерв и прерывает проведение болевого импульса. Эта процедура обычно облегчает боль. Однако иногда боль, спустя некоторое время, возобновляется, а у многих пациентов сохраняется онемение лица или чувство покалывания.
- Баллонная компрессия. При баллонной компрессии, Ваш доктор вводит полую иглу через Ваше лицо в часть нерва, которая выходит на основании черепа. Затем он проводит через иглу тонкую гибкую трубку (катетер) с баллончиком на конце. Врач раздувает баллон с давлением, достаточным для повреждения тройничного нерва и блокировки болевых сигналов. Баллонная компрессия успешно облегчает боль у большинства пациентов, по крайней мере на какой-то период времени. Большинство пациентов после процедуры испытывают онемение лица, а у некоторых отмечается временная или постоянная слабость жевательных мышц.
- Радиочастотное температурное повреждение (деструкция). Процедура избирательно разрушает волокна нерва, связанные с болью. Методика проведения иглы к месту выхода нерва на основании черепа аналогична описанной выше. После расположения иглы через ее просвет проводится электрод, на который подается небольшой электрический ток. Во время процедуры Вас попросят сказать где и когда Вы почувствовали покалывание. Когда же нейрохирург определит часть нерва, вовлеченную в передачу болевых ощущений, электрод разогревается до тех пор, пока это не приводит к разрушению нервных волокон, что создает зону повреждения (деструкции). Если боль сохраняется, врач может создать дополнительные зоны деструкции. Радиочастотная термодеструкция обычно приводит к некоторому онемению лица после процедуры.
- Алкоголизация. Проведение блокады ветвей тройничного нерва в местах их выхода на лице с использованием раствора спирта, которые приводят к разрушению нервных волокон. Методика на сегодняшний день практически утратила свою актуальность ввиду низкой эффективности при таком процессе как лечение невралгии тройничного нерва и высокого процента рецидивов и осложнений. Проведение алкоголизации может иметь смысл, как крайней меры, при невозможности выполнения иных методик.
Очень небольшое количество клинических испытаний было проведено по изучению эффективности альтернативных методов лечения невралгии тройничного нерва, так что убедительных доказательств пользы их применения нет. Однако, некоторые пациенты отмечают улучшение состояния при использовании этих методик. Как правило эффект отмечается при сочетании с традиционными методами лечения.
Альтернативные методики лечения невралгии включают:
- акупунктуру
- витаминотерапию
- рефлексотерапию
- нутрициотерапию
- электростимуляцию нервов
При хронической боли, сопровождающей лечениеи в частности при невралгии тройничного нерва хорошо зарекомендовало себя включение в комплекс лечения психотерапевтических методик.
Всегда необходимо проконсультироваться с Вашим врачом до того, как прибегать к альтернативному лечению, так как в противном случае Вы может усугубить свое состояние.
Развернутую консультацию по поводу Вашего заболевания и ответы на все вопросы Вы можете получить в нашей клинике, которая уже более 20 лет специализируется на лечении такого рода заболеваний и имеет наибольший опыт в Украине
Задайте вопрос специалистам Клиники Субтенториальной нейрохирургии, заполнив поля ниже.
Принципы лечения и ведения больных невралгией тройничного нерва
Л.С. Манвелов, В.М. Тюрников, А.В. Кадыков, НИИ неврологии РАМН, г. Москва, РФ
Невралгия тройничного нерва (НТН) — заболевание, проявляющееся резкой лицевой болью в зонах иннервации его ветвей. Болевые приступы часто провоцируются легким прикосновением к коже так называемых курковых зон: участков губ, крыльев носа, бровей. В то же время, сильное давление на эти зоны облегчает приступ.
Тактика ведения больных НТН должна предусматривать:
• диагностику заболевания, включающую общее клиническое, отоларингологическое, стоматологическое и инструментальное обследование;
• выявление этиологических факторов;
• консервативное лечение;
• хирургическое лечение.
Основными целями лечения НТН являются купирование болевого синдрома и предупреждение рецидивов заболевания.
Консервативное лечение подразумевает лекарственное лечение и физиотерапию.
Примерно в 90% случаев НТН эффективно применение противоэпилептических препаратов. Первым из них был применен фенитоин, однако с 1961 года до настоящего времени широко применяется более эффективное средство — карбамазепин, справедливо считающийся препаратом первого выбора для лечения больных с НТН. Начальная доза составляет 200–400 мг в сутки, постепенно ее увеличивают до прекращения боли, в среднем — до 800 мг в сутки в 4 приема, затем уменьшают до минимально эффективной дозы. При лечении карбамазепином в 70% случаев удается купировать болевой синдром.
Препаратами второго ряда являются фенитоин, баклофен, вальпроевая кислота, тизанидин, антидепрессанты.
Фенитоин при обострениях заболевания назначают в дозе 15 мг/кг внутривенно капельно в течение 2 часов однократно.
Баклофен принимают внутрь во время еды. Начальная доза — 5 мг 3 раза в сутки, последующее увеличение дозы — на 5 мг каждые 3 дня до достижения эффекта, но не более 20–25 мг 3 раза в сутки. Максимальная доза — 100 мг в сутки, назначаемая на короткое время в условиях стационара. Окончательная доза устанавливается так, чтобы при приеме препарата снижение мышечного тонуса не приводило к чрезмерной миастении и не ухудшало двигательные функции. При повышенной чувствительности начальная суточная доза баклофена — 6–10 мг с последующим медленным увеличением. Отменять препарат следует постепенно — в течение 1–2 недель.
Вальпроевая кислота назначается в качестве терапии взрослым в начальной дозе 3–15 мг в сутки в 2 приема независимо от приема пищи. При необходимости дозу препарата увеличивают на 5–10 мг/кг в неделю. Максимальная доза составляет 30 мг/кг в сутки или 3000 мг в сутки. При комбинированном лечении взрослым назначают 10–30 мг/кг в сутки с последующим повышением на 5–10 мг/кг в неделю. Если принимается решение о переходе на внутривенное введение препарата, его выполняют через 4–6 часа после перорального приема в дозе 0,5–1 мг/кг в час.
Тизанидин назначается внутрь. Режим дозирования устанавливают индивидуально. Начальная суточная доза составляет 6 мг (1 капсула). При необходимости суточную дозу можно постепенно увеличивать — на 6 мг (1 капсула) с интервалами 3–7 дней. Для большинства больных оптимальная доза препарата составляет 12 мг в сутки (2 капсулы). В редких случаях может потребоваться увеличение суточной дозы до 24 мг.
Амитриптилин рекомендуется принимать внутрь после еды. Начальная доза взрослым составляет 25–50 мг на ночь, затем дозу увеличивают в течение 5–6 дней до 150–300 мг в сутки в 3 приема. Большая часть дозы принимается на ночь. Если в течение 2 недель не наступает улучшение, суточную дозу увеличивают до 300 мг. Больным в пожилом возрасте при легких нарушениях препарат назначается в дозе 30–100 мг на ночь. После достижения терапевтического эффекта переходят на минимальные поддерживающие дозы — 25–50 мг в сутки. Амитриптилин вводят внутримышечно или внутривенно капельно в дозе 25–40 мг 4 раза в сутки, постепенно заменяя приемом внутрь. Длительность лечения составляет не более 8–10 месяцев [2, 3].
Показана витаминотерапия, в основном — применение витаминов группы В. Хорошо зарекомендовали себя комбинированные препараты.
Прием анальгетиков считается малоэффективным. К тому же, употребление больших доз этих препаратов, связанное с желанием быстро купировать приступ, может привести к появлению абузусной головной боли.
Из физиотерапевтических методов в острый период заболевания и во время приступа показано умеренное тепловое воздействие: лампа «Соллюкс», электрическая грелка, ультрафиолетовое облучение больной половины лица. Анальгезирующее и противовоспалительное действие оказывают широко применяющиеся диадинамические токи. На курс лечения назначают 6–10 процедур, которые проводят ежедневно. Рекомендуют 2–3 таких курса с перерывом в 1 неделю. Кроме того, эту процедуру в течение 2–3 минут проводят на области височной артерии и звездчатого узла. При упорной боли с помощью диадинамических и синусоидальных модулированных токов вводят прокаин, тетракаин, эпинефрин. Анестезирующий эффект при этом выражен больше, чем при использовании гальванического тока. При длительном упорном болевом синдроме, хроническом течении заболевания увеличивают время воздействия диадинамическими токами до 8–10 минут. На курс лечения назначают 10–18 процедур с 4-дневным перерывом после 10 сеансов.
При лицевой боли, связанной с шейным остеохондрозом, симпатико-радикулярным симптомокомплексом хороший эффект дает воздействие ультразвуком не только паравертебрально, но и на места выхода тройничного нерва по 2 минуты на каждую точку через день. В результате такого воздействия лицевая боль не возобновлялись в течение 1 года после лечения [4]. Противопоказаниями к лечению ультразвуком являются склонность к носовым кровотечениям, отслойка сетчатки глаза, острые воспалительные процессы в носовых пазухах, среднем ухе, нарушения мозгового кровообращения. В период лечения ультразвуком уменьшается не только болевой синдром, но и регионарные и общие вегетативно-сосудистые нарушения.
В подострый период при наличии триггерных зон применяется эндоназальный электрофорез 4% раствора прокаина и 2% раствора тиамина, продолжительность воздействия составляет от 10 до 30 минут. Кроме того, его можно осуществлять в виде полумаски и маски Бургонье (при двустороннем поражении нервов). Применяется также электрофорез дифенгидрамина, пахикарпина гидройодида, платифиллина на больную сторону лица. При артрозе височно-нижнечелюстного сустава проводят электрофорез метамизола натрия, гиалуронидазы; при ревматической этиологии заболевания — салицилатов; при малярийной — хинина; при обменных нарушениях — йода и прокаина.
Эффективно также применение электрического поля ультравысоких частот в олиготермической дозе.
При хронических формах НТН, шейном остеохондрозе с лицевой болью тригеминального характера назначают массаж лица по 6–7 минут ежедневно или через день. Положительное воздействие оказывают грязевые аппликации на воротниковую область при температуре 36–37°С по 10 минут. На курс назначают 10 процедур. Используют озокерит, парафин или торф. Успешно применяют бальнеотерапию: сульфидные, морские, радоновые ванны. Нельзя переоценить благотворное воздействие лечебной гимнастики. Санаторно-курортное лечение в санаториях для больных с заболеваниями периферической нервной системы рекомендуют в теплое время года при хроническом течении заболевания и редких приступах. Положительно влияет рефлексотерапия (иглоукалывание, прижигание, лазеротерапия).
Если консервативная терапия оказывается неэффективной или наблюдаются выраженные побочные действия лекарств — обсуждается необходимость хирургического вмешательства.
В 1884 году американский хирург Д.Э. Мирс при хронической НТН впервые произвел удаление его ганглия. В 1890 году английский хирург У. Рос и американский хирург Э. Эндерюс независимо друг от друга разработали специальный метод удаления гассерова узла, который вошел в практику нейрохирургов в конце XIX и начале XX вв. В настоящее время при НТН используются следующие способы оперативного вмешательства:
• микрохирургическая декомпрессия нерва на выходе из ствола мозга;
• частичная сенсорная ризотомия;
• периферическая блокада или перерезка нерва проксимальнее узла Гассера;
• нейроэктомия;
• криохирургические методы;
• диатермокоагуляция;
• высокочастотное излучение.
Наиболее распространенными современными эффективными методами хирургического лечения НТН являются микроваскулярная декомпрессия и пункционные деструктивные операции. Среди деструктивных операций, входящих в состав арсенала хирургических вмешательств при НТН, выделяют чрескожную высокочастотную селективную ризотомию (ЧВСР), баллонную микрокомпрессию и глицероловую ризотомию [8].
Наиболее распространенным деструктивным методом является ЧВСР, представляющая собой контролируемую термическую деструкцию гассерова узла, которая препятствует передаче сенсорных импульсов и развитию болевых пароксизмов. Локация электрода контролируется по отношению к порциям узла. Этот метод успешно применяется в ведущих клиниках, занимающихся проблемой боли [1, 6, 7].
Значительный опыт ЧВСР накоплен в Mayfield Clinik Chincinati (доктор медицины John Tew). В этой клинике с использованием данного метода прооперировано более 3 тысяч больных. Хорошие результаты были получены у 93% больных. Рецидивы боли в течение 15 лет наблюдались у 25% больных [7]. Рецидивы болезни в течение первых 5 лет отмечены у 15% больных, до 10 лет — у 7%, от 10 до 15 лет — у 3% больных. Отмечается прямая связь между выраженностью гипалгезии после чрескожной ризотомии, частотой рецидивов боли и дизестезий. При достижении легкой гипалгезии после операции и наблюдении в течение 3 лет частота рецидивов боли достигала 60%, при этом дизестезии наблюдаются у 7% больных. При достижении выраженной гипалгезии и наблюдении больных в течение 15 лет частота рецидивов боли составила 25%, вероятность дизестезий увеличилась до 15%. При получении полной аналгезии после чрескожной ризотомии и наблюдении больных в течение 15 лет частота рецидивов боли наблюдалась в 20% случаев, число дизестезий увеличилось до 36%. Таким образом, наиболее благоприятным является второй вариант — достижение выраженной гипалгезии.
К сожалению, в нейрохирургические отделения довольно часто попадают больные с запущенными формами НТН, в том числе после многочисленных деструктивных процедур. Несомненно, это ухудшает функциональный результат нейрохирургических вмешательств и в некоторых случаях требует сложных и более опасных операций на уровне центральной нервной системы [1, 5].
Преимущества ЧВСР: бескровность, быстрота и безопасность вмешательства, местная анестезия в качестве обезболивания и, наконец, высокий процент положительных результатов. ЧВСР гассерова узла при НТН и кластерной головной боли является высокоэффективным и безопасным методом хирургического вмешательства.
Обострения заболевания чаще всего бывают весной и осенью. При отсутствии рецидивов прогноз благоприятный.
Список литературы
Григорян Ю.А. Чрескожная высокочастотная, селективная ризотомия и микроваскулярная декомпрессия корешка тройничного нерва в лечении тригеминальной невропатии: Автореф. дис. … канд. мед. наук. – М., 1989. Кадыков А.С., Шахпаронова Н.В., Манвелов Л.С. Невралгия тройничного нерва. В кн.: Практическая неврология / Под ред. А.С. Кадыкова, Л.С. Манвелова, В.В. Шведкова. – М.: ГЭОТАР-Медиа, 2011. – С. 26–27. Лекарственные средства / Под ред. Р.У. Хабриева, А.Г. Чучалина. – М.: ГЭОТАР-Медиа, 2006. – 753 с. Стрелкова Н.И. Физические методы лечения в неврологии. – М.: Медицина, 1991. – С. 134–137. Оглезнев К.Я., Григорян Ю.А., Шестериков С.А. Патофизиологические механизмы возникновения и методы лечения лицевых болей. – Новосибирск: Наука, 1990. – 192 с. Broggi G., Franzini A., Lasio G. et al. Long time results of percutaneous retrogasserian Thermorhizotomy for essential trigeminal neuralgia consdarations in 1000 patients // Nerosurgery. – 1995. – Vol. 83. – P. 989–993. Taha J.M., Bumer U.R. A prospective 15-year follow up of 154 consecutive patients with trigeminal neuralgia treated by percutaneous stereotactic radiofre-quensy thermal rhizotomy // J. Neurosurgery. – 1995. – Vol. 83. – Р. 989–993. Wegel G., Kasey K. Strring Back Trigeminal neuralgia Association. 2000.Ранее статья была опубликована в РМЖ, 2014, №16
Ваше полное руководство по невралгии тройничного нерва; A. M. Kaufmann & M. Patel, CCND Winnipeg
Ваше полное руководство по невралгии тройничного нерва; А. М. Кауфманн и М. Патель, CCND ВиннипегЧасть вторая: Лечение невралгии тройничного нерва
II. Лекарства А. Введение Сегодня невралгия тройничного нерва обычно лечится препаратами, называемыми противосудорожными, в том числе карбамазепином. (Тегретол), фенитоин (Дилантин), оксикарбазепин (Трилептал) , и габапентин (Нейронтин).Фенитоин был впервые представлен в 1942 г. а в 1962 году карбамазепин стал наиболее распространенным использованный препарат. Баклофен (Лиорезал) может повысить эффективность этих препаратов. В последнее время широко используется нейронтин (габапентин). из-за меньшего количества побочных эффектов, хотя стоит дороже и несколько дешевле эффективен тогда Тегретол. Противосудорожные средства Считается, что уменьшает приступы TN за счет снижения гиперактивности тройничного нерва нервное ядро в стволе головного мозга. Лечение обычно начинают с одного препарата, например
как Тегретол или Нейронтин.Дозу увеличивают по мере необходимости и переносимости. Если какой-либо отдельный препарат окажется неэффективным,
альтернативные препараты можно попробовать отдельно или в комбинации с другими препаратами. Медицинский
терапия изначально эффективна для большинства пациентов с ТН. К сожалению, около
половина пациентов, страдающих TN, в конечном итоге становятся недовольными медикаментозной терапией, потому что
неполного контроля боли или побочных эффектов, связанных с лекарствами, которые почти всегда
опытный. Затем рассматривается возможность хирургического лечения.
| Нервно-сосудистая система сдавление зоны входа корешка тройничного нерва приводит к гиперактивности ядра тройничного нерва. | Медицинский терапия направлена на снижение гиперактивности ядра тройничного нерва, тем самым уменьшая приступы боли TN. |
Почти все типовые Больные TN испытывают значительное облегчение боли при приеме карбамазепина. В начальная суточная доза низкая (от одной до двух таблеток в день), которую постепенно увеличивают. до тех пор, пока боль не исчезнет полностью или не возникнут побочные эффекты.Хорошее облегчение боль может быть достигнута при низких дозах, но обычная эффективная доза колеблется от От 600 до 1600 мг, разделенных на три или четыре приема в день. Даже более высокие дозы могут потребуются при сильных приступах боли. Как только облегчение боли было достигнута, та же доза обычно сохраняется в течение как минимум двух недель перед попыткой снизить до минимальной дозировки, обеспечивающей обезболивание. Как и все препараты TN, В периоды ремиссии можно постепенно снижать содержание тегретола.
Несколько дозозависимых часто наблюдаются побочные эффекты, включая сонливость, спутанность сознания, головокружение, нистагм (быстрые движения глаз), атаксия (снижение координации), диплопия (двоение в глазах), тошнота и анорексия (потеря аппетита).Если побочные эффекты тяжелая, суточная доза карбамазепина может быть уменьшена в течение 1-3 дней, прежде чем пытаясь снова увеличить суточную дозу.
Карбамазепин вызывает также редкие, но серьезные реакции.
которые не зависят от дозы. К ним относятся аллергическая кожная сыпь, которая может образовывать
в любое время после начала приема лекарства. От двух до шести процентов больных, которые
принимать карбамазепин, развиваться заболевания крови, включая лейкопению или агранулоцитоз
(падение количества лейкоцитов) или апластическая анемия (когда костная
костный мозг перестает производить клетки крови).Другие редкие осложнения включают токсичность печени, водную интоксикацию (задержку воды), гипонатриемию (низкий уровень натрия в крови), застойные явления.
сердечная недостаточность, зрительные галлюцинации и расстройства вкуса или половой функции.
Из-за этих осложнений перед приемом карбамазепина обычно проводят анализы крови.
запускается и периодически повторяется. Прием карбамазепина
следует прекратить, если количество лейкоцитов станет аномально низким.
Следует немедленно уведомить врача и провести анализы крови, если
испытывает жар, боль в горле, стоматит (болезненное инфицирование ротовой полости),
легкие синяки или петехии (крошечные красные пятна на коже).
Оксикарбамазепин это новая форма Тегретола®, которая может иметь меньше побочных эффектов и рисков. токсичности, но должны приниматься в более высоких дозах, чтобы обеспечить адекватный контроль боли.
С. Трилептал (оксикарбазепин)Трилептал, или оксикарбемазепин, представляет собой форму Тегретола®, которая получает все более широкое распространение назначают при различных состояниях. Недавно было обнаружено, что он эффективен для некоторых пациентов с невралгией тройничного нерва.Как и Тегретол®, это противосудорожное средство. препарата, но побочные эффекты менее серьезны и возникают реже.
Доза обычно начинается с 300 мг. два раза в день и постепенно увеличивают для достижения контроля боли. Максимум доза составляет 2400-3000 мг в сутки. Общие побочные эффекты — тошнота, рвота, головокружение, утомляемость и тремор. Менее частые симптомы — сыпь, респираторные инфекции, двоение в глазах и изменение электролитов в крови. Если у вас была аллергия реакция на Тегретол® (карбемазепин), то не следует пробовать Трилептал.Как и в случае с другими противосудорожными препаратами, следует увеличивать и уменьшать дозу. быть постепенным.
Д. Фенитоин (дилантин)фенитоин снимает тик боль более чем у половины пациентов с ТН в дозах от 300 до 500 мг, разделенных на три приема в день. Фенитоин также может вводить внутривенно для лечения тяжелых обострений TN. Максимум доза зависит от серьезности побочных эффектов, которые испытывает Наркотик.Эти дозозависимые побочные эффекты включают нистагм (быстрые движения глаза), атаксия (снижение координации), дизартрия (затруднение речи), офтальмоплегия (паралич движений глаз), а также сонливость и психические расстройства. путаница. Другие эффекты лекарства могут включать гиперплазию десен. (увеличение десен во рту) и гипертрихоз (чрезмерный рост волос). Могут возникнуть редкие, но серьезные осложнения, включая аллергические высыпания на коже, печени. повреждения и нарушения со стороны крови.
E. Baclophen (Lioresal)
Баклофен не так эффективен, как карбамазепин или фенитоин, для TN, но может использоваться в сочетание с этими лекарствами. Начальная доза баклофена обычно составляет 5 мг два или три раза в день, можно постепенно увеличивать. Обычная дозировка для полного обезболивания принимают от 50 до 60 мг в день. Баклофен имеет короткая продолжительность функции, поэтому пациентам с тяжелым TN может потребоваться прием доз каждые 3-4 часа.
Наиболее частые побочные эффекты, связанные с баклофеном, включают сонливость, головокружение, тошнота и слабость в ногах. Частота возникновения этих побочных эффектов снижается, если начинать с низкой дозой баклофена, которую постепенно увеличивают. Однако примерно одна десятая часть больных не переносит баклофен. Редкое осложнение — сбивающее с толку состояние, которое появляется вскоре после начала приема баклофена, но быстро проходит при прекращении терапии. Не следует прекращать прием Баклофена сразу после длительное использование, потому что могут возникнуть галлюцинации или судороги.Если эти изъятия симптомы действительно возникают, обычно восстанавливают предыдущую дозу баклофена и затем постепенно снижается.
Габапентин Ф. (Нейронтин)
Габапентин является противоэпилептическим препаратом, структурно связанным с нейромедиатором ГАМК. Этот препарат почти так же эффективен, как карбамазепин. но вызывает меньше побочных эффектов. начальная доза обычно составляет 300 мг три раза в день, и ее увеличивают до максимальная доза.Наиболее частые побочные реакции включают сонливость (сонливость), атаксия (снижение координации), утомляемость и нистагм (быстрые движения глаз). Нет данных о взаимодействии с Тегретолом. или Дилантин, что позволяет использовать эти препараты в комбинации с нейронтином. Как и в случае со всеми этими препаратами, следует незамедлительно отменить прием. следует избегать, так как могут возникнуть тяжелые реакции отмены.
Следующий раздел >>
<< Вернуться к содержанию
Нажмите
здесь, чтобы вернуться на веб-сайт
Невралгия тройничного нерва
в Центре
заболеваний черепных нервов
А.М. Кауфманн и М. Патель
Центр заболеваний черепных нервов
Виннипег, Манитоба, Канада
© 2001
Подготовлено A. М. Кауфманн и М. Пател
© 2001 Центр заболеваний черепных нервов, Виннипег, Университет Манитобы, Центр медицинских наук. Информация, представленная на этом сайте, предназначена только в образовательных целях и не должны использоваться для диагностики или лечения заболевания. или беспорядок. Эта информация не предназначена для замены, дополнения или каким-либо образом квалифицировать услуги или советы, предоставленные квалифицированным специалистом в области здравоохранения.Пожалуйста, проконсультируйтесь с сертифицированным специалистом в области здравоохранения, прежде чем заполнять какую-либо форму. лечебного действия. Копирование в любой части или форме этого документа строго запрещено. запрещенный. Все права защищены. Для получения дополнительной информации ознакомьтесь с нашим заявлением об отказе от ответственности . По вопросам, связанным с веб-сайтом, можно обращаться по номеру Information Провайдер .
Противосудорожные средства, релаксанты скелетных мышц, трициклические антидепрессанты, токсины
Автор
Manish K Singh, MD Ассистент-профессор кафедры неврологии, преподавательский факультет программы резидентуры по лечению боли и неврологии, Университетская больница Ганемана, Медицинский колледж Дрекселя; Медицинский директор, неврология и лечение боли, Институт нейробиологии Джерси
Маниш К Сингх, доктор медицины, является членом следующих медицинских обществ: Американской академии неврологии, Американской академии медицины боли, Американского общества головной боли, Американской ассоциации врачей индийского происхождения , Американская медицинская ассоциация, Американское общество региональной анестезии и медицины боли
Раскрытие: Ничего не разглашать.
Соавтор (ы)
Гордон Х. Кэмпбелл, MSN, FNP-BC Практикующая медсестра, неврологическая служба, Портлендский медицинский центр по делам ветеранов; Начальный факультет, клинический инструктор и приглашенный лектор, Отделение семейного ухода, Школа медсестер Университета медицинских наук штата Орегон
Гордон Х. Кэмпбелл, MSN, FNP-BC является членом следующих медицинских обществ: Американская академия неврологии
Раскрытие информации: ничего расскрыть.
Сиддхарт Гаутам, врач-резидент MBBS , Институт нейробиологии Джерси
Раскрытие информации: раскрывать нечего.
Helmi L Lutsep, MD Профессор и заместитель председателя кафедры неврологии Медицинского факультета Орегонского университета здоровья и науки; Заместитель директора Центра инсульта OHSU
Хелми Л. Луцеп, доктор медицины, является членом следующих медицинских обществ: Американская академия неврологии, Американская ассоциация инсульта
Раскрытие информации: Medscape Neurology Редакционный консультативный совет: Комитет по рассмотрению инсульта, CREST2; Консультативный совет врачей Coherex Medical; Клиническое испытание национального лидера и руководящего комитета, Bristol Myers Squibb; Abbott Laboratories, консультативная группа.
Главный редактор
Роберт Эган, MD NW Neuro-Ophthalmology
Роберт Эган, доктор медицины, является членом следующих медицинских обществ: Американская академия неврологии, Американская кардиологическая ассоциация, Североамериканское нейроофтальмологическое общество, Медицинская ассоциация Орегона
Раскрытие информации : Получил гонорары от Biogen Idec и Genentech за участие в консультативных советах.
Благодарности
Джейн В. Чан, доктор медицины Профессор неврологии / нейроофтальмологии, медицинский факультет, отделение неврологии, медицинский факультет Университета Невады
Джейн В. Чан, доктор медицины, является членом следующих медицинских обществ: Американской академии неврологии, Американской академии офтальмологии, Американской медицинской ассоциации, Североамериканского нейроофтальмологического общества и Phi Beta Kappa
.Раскрытие: Ничего не нужно раскрывать.
Джеймс Р. Коуч, доктор медицинских наук, FACP Профессор неврологии, Центр медицинских наук Университета Оклахомы
Раскрытие: Ничего не нужно раскрывать.
Теодор Дж. Гаэта, DO, MPH, FACEP Доцент кафедры неотложной медицины Медицинского колледжа Вейл Корнелл; Заместитель председателя и директор программы резидентуры по неотложной медицине, Департамент неотложной медицины, Методистская больница Нью-Йорка; Научный руководитель, адъюнкт-профессор кафедры неотложной медицины, медицинский факультет Университета Святого Георгия
Теодор Дж. Гаэта, DO, MPH, FACEP является членом следующих медицинских обществ: Альянса клинического образования, Американского колледжа врачей неотложной помощи, руководителей отделов неотложной медицины, Совета директоров резиденций неотложной медицины, Нью-Йоркской медицинской академии и Общество академической неотложной медицины
Раскрытие: Ничего не нужно раскрывать.
Дж. Стивен Хафф, доктор медицины Доцент кафедры неотложной медицины и неврологии, факультет неотложной медицины, Медицинский факультет Университета Вирджинии
Дж. Стивен Хафф, доктор медицинских наук, является членом следующих медицинских обществ: Американской академии неотложной медицины, Американской академии неврологии, Американского колледжа врачей неотложной помощи и Общества академической неотложной медицины
Раскрытие: Ничего не нужно раскрывать.
Саймон К. Ло, доктор медицинских наук, фармацевт является членом следующих медицинских обществ: Американской академии офтальмологии, Американского общества глаукомы и Ассоциации исследований в области зрения и офтальмологии
Раскрытие: Ничего не нужно раскрывать.
Эндрю Лоутон, доктор медицины Медицинский директор нейроофтальмологической службы, отделение офтальмологии, Баптистский глазной центр, Баптистский медицинский медицинский центр
Эндрю Лоутон, доктор медицины, является членом следующих медицинских обществ: Американской академии офтальмологии, Медицинского общества Арканзаса и Южной медицинской ассоциации
Раскрытие: Ничего не нужно раскрывать.
Марк Э. Ленертс, доктор медицины, FAHS Штатный невролог, Mercy Medical Group; Адъюнкт-клинический профессор неврологии, кафедра неврологии, Калифорнийский университет, Дэвис, медицинский факультет
Марк Э. Ленертс, доктор медицины, FAHS является членом следующих медицинских обществ: Американской академии неврологии, Американского общества головной боли и Международного общества головной боли
Раскрытие: Ничего не нужно раскрывать.
Хорхе Э. Мендизабал, MD Консультант, Корпус Кристи Неврология
Хорхе Э. Мендизабал, доктор медицины, является членом следующих медицинских обществ: Американской академии неврологии, Американского общества головной боли, Национальной ассоциации инсульта и Совета по инсульту Американской кардиологической ассоциации
Раскрытие: Ничего не нужно раскрывать.
Hampton Roy Sr, MD Доцент кафедры офтальмологии Медицинского университета Арканзаса
Хэмптон Рой-старший, доктор медицины, является членом следующих медицинских обществ: Американской академии офтальмологии, Американского колледжа хирургов и Панамериканской ассоциации офтальмологов
Раскрытие: Ничего не нужно раскрывать.
Tom Scaletta, MD Заведующий отделением неотложной медицины, больница Эдварда; Бывший президент Американской академии экстренной медицины
Том Скалетта, доктор медицины, является членом следующих медицинских обществ: Американская академия экстренной медицины
Раскрытие: Ничего не нужно раскрывать.
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Medscape Salary Employment
Brian R Younge, MD Профессор офтальмологии, Медицинский факультет клиники Майо
Брайан Р. Юнг, доктор медицины, является членом следующих медицинских обществ: Американской медицинской ассоциации, Американского офтальмологического общества и Североамериканского нейроофтальмологического общества
Раскрытие: Ничего не нужно раскрывать.
«Молния боли»
Фарм США . 2017; 42 (1): 41-44.
РЕФЕРАТ: Невралгия тройничного нерва (TGN) — это внезапно возникающая, кратковременная, но изнурительная нейропатическая боль, возникающая в результате сжатия пятого черепного нерва, вызванная повседневными действиями, такими как жевание и речь. Это хроническое заболевание чаще всего встречается у пожилых женщин, поражая до 27 на 100 000 человек во всем мире. Фармакологическим препаратом первой линии для TGN является противосудорожное средство карбамазепин, с окскарбазепином, используемым по аналогичному механизму, но с более мягким профилем побочных эффектов.Лекарственные препараты второго ряда (баклофен, ламотриджин) считаются полезными вспомогательными средствами, а менее изученные лекарства или хирургическое вмешательство прибегают к помощи, если только стандартное лечение неэффективно или не переносится пациентом.
Невралгия тройничного нерва (TGN), или tic douloureux , представляет собой быстрое начало колющей, односторонней лицевой боли, длящейся от нескольких секунд до минут, вызванное простыми действиями, такими как прием пищи, чистка зубов, разговор или воздействие порыв холодного воздуха.По оценкам, TGN поражает приблизительно от 12,6 до 27 человек на 100 000 человек во всем мире 1,2 и наиболее часто встречается у женщин в возрасте старше 50 лет. 3 В США распространенность TGN составляет 15,5 случаев на 100 000 человек. 4
Эта «молния» боли исходит от пятого черепного нерва, который имеет три отдела, обеспечивающих чувствительность различных участков лица. Офтальмологический нерв (V 1 ) поддерживает ощущения в глазах и лбу, верхнечелюстной нерв (V 2 ) в области щек и верхней губы, а нижнечелюстной нерв (V 3 ) иннервирует область челюсти, которая участвует в кусании, жевании и глотании.Боль TGN исходит из верхнечелюстного и нижнечелюстного отделов. TGN ассоциируется с более высоким уровнем депрессии, поскольку на качество жизни пациента может влиять хроническая боль, и могут потребоваться антидепрессанты. 5
Патогенез и диагностикаМеханизмы, участвующие в патогенезе TGN, до конца не изучены. Считается, что сдавление сосудов, обычно венозных или артериальных петель на входе тройничного нерва в мост, приводит к очаговой демиелинизации тройничного нерва. 6-8 TGN подразделяется на три категории: идиопатический не имеет четкой причины, классический вызван компрессией V черепного нерва и вторичный является результатом основного заболевания, такого как опухоль головного мозга или рассеянный склероз. 9 Клинические данные, анамнез и подробное обследование головы, шеи, зубов и челюсти остаются основными методами исключения других причин невропатической боли. Нейровизуализация с помощью МРТ используется в диагностике при подозрении на сдавление нерва или при необходимости хирургического вмешательства.Медикаментозная терапия остается основным методом лечения ТГН.
Медикаментозная терапия первого рядаКарбамазепин: На основании клинических исследований карбамазепин является признанным вариантом лечения первого ряда для TGN; это также единственный одобренный FDA препарат со специальными показаниями для TGN. 10-13 Обычная начальная доза карбамазепина составляет от 100 до 200 мг два раза в день при пероральном приеме, которая может быть увеличена по мере переносимости до поддерживающей дозы от 600 до 800 мг в день в разделенных дозах.Максимальная доза не должна превышать 1200 мг в день. Эти медленные титрования дозы уменьшают эффекты центральной нервной системы (ЦНС), такие как сонливость, головокружение, атаксия и нистагм. Карбамазепин — это блокатор потенциал-управляемых натриевых каналов, который останавливает распространение потенциала действия, механизма лечения эпилепсии. Ингибирование этого «повторяющегося возбуждения» делает карбамазепин подходящим основным средством лечения ТГН. Карбамазепин также показан для лечения пациентов с биполярным расстройством, которые не могут переносить другие лекарства от мании, такие как литий или вальпроат. 10-13
Карбамазепин может изменять состояние костного мозга, приводя к уменьшению количества эритроцитов, лейкоцитов и тромбоцитов, состояние, известное как апластическая анемия . Таким образом, пациенты должны быть проинформированы о признаках и симптомах миелосупрессии, при этом обычные клинические анализы крови выполняются в течение первых 3 месяцев лечения, а частота определяется по результатам. 14 Карбамазепин стимулирует высвобождение антидиуретического гормона (АДГ), усиливая реабсорбцию воды и повышая вероятность гипонатриемии, что может иметь негативное влияние на пожилых пациентов, получающих лечение от ТГН.В этой популяции также могут наблюдаться изменения минерализации костей, поскольку наблюдалось снижение уровня витамина D при хроническом введении карбамазепина. 15
Карбамазепин является хорошо известным индуктором CYP450 3A4, при этом сообщалось о значительных лекарственных взаимодействиях, таких как снижение эффективности варфарина или пероральных контрацептивов. 16 Более высокие уровни карбамазепина в сыворотке крови возникают, если препарат одновременно вводится с ингибиторами CYP450, включая макролидные антибиотики, вальпроат, азольные противогрибковые средства и грейпфрутовый сок.Эти эффекты, вместе взятые, могут быть проблематичными для врача, лечащего пожилого пациента, у которого частота TGN является самой высокой. 17
Карбамазепин противопоказан лицам из восточной и юго-восточной Азии, у которых был положительный результат теста на аллель HLA-B * 15: 02. 18 Эти люди подвержены повышенному риску развития синдрома Стивенса-Джонсона (SJS) и токсического эпидермального некролиза (TEN). Хотя эта реакция маловероятна, она фатальна, и при появлении сыпи следует немедленно прекратить прием карбамазепина.
Окскарбазепин: Окскарбазепин является кето аналогом карбамазепина, пролекарства, превращенного в активный метаболит, 10-моногидроксипроизводное. Препарат начинают с пероральной дозы 600 мг в день, затем ее увеличивают на 300 мг до общей суточной дозы от 1200 до 1800 мг в день. Механизм действия такой же, как у карбамазепина, но окскарбазепин также снижает активность высоковольтных кальциевых каналов. Окскарбазепин имеет меньше побочных эффектов и лекарственных взаимодействий, чем карбамазепин, и является подходящей альтернативой для пациентов пожилого возраста с нарушениями функции почек, печени и сердца.Поскольку окскарбазепин является аналогом карбамазепина, его также следует избегать у пациентов, экспрессирующих генетический аллель HLA-B * 15: 02 из-за редкой кожной реакции. 19,20
Таким образом, карбамазепин и окскарбазепин остаются золотым стандартом фармакотерапии TGN. Противосудорожные препараты следует тщательно титровать, часто отслеживая побочные эффекты и лекарственные взаимодействия. ТАБЛИЦА 1 обобщает карбамазепин и окскарбазепин как препараты первой линии для лечения ТГН.
Медикаментозная терапия второй линииСледующие препараты предназначены для пациентов, которые не реагируют на карбамазепин и окскарбазепин, или имеют опасения по поводу побочных эффектов или лекарственных взаимодействий, поскольку они считаются вспомогательными для лечения TGN . Кроме того, имеется меньше исследований, подтверждающих их эффективность.
Ламотриджин: Ламотриджин — это противосудорожное средство, которое подавляет быстрое возбуждение нейронов и вызывает зависимую от напряжения и потребления блокаду натриевых (Na + ) каналов, стабилизируя нейронные мембраны.Также наблюдается снижение высвобождения глутамата, возбуждающего нейромедиатора. Для TGN ламотриджин обеспечивает эффективную дополнительную терапию. 21 Ламотриджин вводят перорально в суточной дозе 25 мг в течение первых 2 недель, а затем ее увеличивают до 50 мг в сутки в течение 3 и 4 недель, пока общая доза ламотриджина не достигнет 400 мг в сутки (в два приема). Пациентам, получающим параллельную терапию индукторами CYP3A4, следует начинать с ламотриджина в дозе 50 мг один раз в день, постепенно увеличивая дозу до 100 мг один раз в день на 3 неделе, 200 мг один раз в день на 5 неделе, 300 мг один раз в день на 6 неделе. и 400 мг один раз в день на 7 неделе.Пациентам, принимающим ингибитор CYP3A4, следует начинать с более низкой дозы (12,5-25 мг) через день и увеличивать ее на 25 мг каждые 2 недели до 400 мг в день. Сообщалось о потенциально смертельных кожных реакциях при лечении ламотриджином, особенно в первые недели терапии, и пациенты должны быть проинструктированы о необходимости незамедлительно прекратить прием препарата при первых признаках сыпи. 22
Баклофен: Баклофен является релаксантом скелетных мышц, действующим как агонист гамма-аминомасляной кислоты типа B (GABA B ).Лечение баклофеном позволяет увеличить приток хлорид-ионов и закрыть пресинаптические кальциевые каналы, что снижает высвобождение возбуждающих передатчиков в ЦНС для уменьшения мышечных спазмов. Для купирования боли баклофен снижает содержание вещества P в спинном мозге. Начальная доза баклофена для ТГН составляет 15 мг в день перорально в три приема с постепенным титрованием до поддерживающей дозы от 50 до 60 мг в день. При ТГН баклофен снижает количество болезненных эпизодов и продлевает ремиссию. 23
Усиливая действие ГАМК, баклофен может вызывать сонливость и угнетение дыхания в случае передозировки. Прием препарата следует постепенно снижать, и не рекомендуется резкая отмена, поскольку могут возникнуть спастичность, галлюцинации и судороги. 24
ТАБЛИЦА 1 суммирует действия ламотриджина и баклофена в качестве лекарственной терапии второй линии для TGN.
Рефрактерная терапияГабапентин: Габапентин является аналогом ГАМК, ценным для лечения невропатической боли. 25 Препарат модулирует высвобождение ГАМК без прямого рецепторного действия. В ЦНС габапентин связывает кальциевые каналы N-типа, что приводит к уменьшению поступления кальция в нейроны. Габапентин начинают перорально в дозе 300 мг в день для TGN и могут быть увеличены на 300 мг каждые 2–3 дня по мере переносимости. Максимальная суточная доза габапентина составляет 1800 мг. Наиболее частыми эффектами, связанными с габапентином, являются сонливость, головокружение, атаксия, головная боль и тремор. С этим аналогом ГАМК связаны минимальные лекарственные взаимодействия.
Ботулинический токсин типа А (Ботокс-А): Ботокс-А оказался эффективным средством лечения нескольких неврологических патологий, включая головную боль. 26-28 Он предотвращает зависимое от кальция высвобождение ацетилхолина, вызывающее расслабление мышц. Хотя эффективность этого токсина в отношении TGN полностью не изучена, считается, что высвобождение ноцицептивных модулирующих пептидов ингибирует центральную и периферическую сенсибилизацию. 29
В нескольких клинических исследованиях стандартная доза Ботокса-А для лечения ТГН составляла от 25 до 100 Ед, вводимых в триггерные зоны, с обезболивающим эффектом до 12 недель.Сообщенные побочные эффекты включали асимметрию лица и отек в месте инъекции, которые переносились пациентами с коротким периодом восстановления. 30-32 Потребуются дальнейшие исследования для установления долгосрочного клинического исхода ботокса-А при лечении TGN.
Другие агенты: Пациенты могут испытывать резкую боль или увеличенную продолжительность и интенсивность TGN, что требует использования сильнодействующих опиоидных анальгетиков, таких как морфин или оксикодон.Проблема с использованием агонистов мю-опиоидных рецепторов остается потенциальной причиной сильного седативного эффекта, зависимости и угнетения дыхания в случае передозировки. 33
Было обнаружено, что пимозид, блокатор дофамина, имеет некоторое преимущество для TGN, который не реагирует на терапию первой линии карбамазепином. 34 Однако этот антагонист дофамина 2 (D 2 ) вызывает экстрапирамидные эффекты и сердечную аритмию, особенно у пожилых пациентов. 34 Таким образом, большинство клиницистов избегают приема пимозида при терапии TGN.
Лидокаин — блокатор натриевых каналов, который останавливает распространение потенциала действия в центральной и периферической нервной системе. Фармакокинетика этого анестетика ограничивает его использование, так как его короткий период полувыведения сокращает продолжительность обезболивания лидокаином до не более 24 часов при внутривенном введении для TGN. 35 Кроме того, более высокие дозы лидокаина могут снижать проводимость миокарда и вызывать тремор и аномальные ощущения в конечностях. 35
Фосфенитоин является пролекарством противосудорожного фенитоина. Пациенты, которые стали невосприимчивыми к пероральным лекарствам и поступили в острый кризис TGN, могут испытывать облегчение боли в течение примерно 48 часов с помощью этого блокатора натриевых каналов, пока не будут рассмотрены другие фармакотерапевтические агенты или пока не будет обеспечено обезболивание перед хирургическим вмешательством. 36
Операция: Операция предназначена для пациентов, которые безуспешно испробовали как минимум три препарата или не могут переносить побочные эффекты или взаимодействия лекарств.Хирургическое вмешательство следует тщательно продумать, так как некоторые процедуры являются инвазивными, требуют анестезии и увеличивают вероятность инфекций. Наиболее часто используемые методы включают микрососудистую декомпрессию, ризотомию и радиохирургию гамма-ножом. 37
ЗаключениеФармакологическая терапия остается исходным лечением для пациентов с ТГН, при этом противосудорожный карбамазепин является общепринятой терапией первой линии. Препараты второго ряда добавляются, если пациент не может переносить побочные эффекты или лекарственные взаимодействия.Фармацевты играют уникальную роль в наблюдении за пациентом на предмет этих исходов. Клинические исследования расширили возможную роль других лекарств для лечения этой нейропатической боли, и эти механизмы должны быть дополнительно оценены как варианты лечения этой хронической боли в будущем.
ССЫЛКИ 1. Купман Дж. С., Дилеман Дж. П., Хюйген Ф. Дж. И др. Частота лицевых болей среди населения в целом. Боль . 2009; 147 (1-3): 122-127.
2. Холл GC, Кэрролл Д., МакКуэй Х.Дж.Заболеваемость первичной медико-санитарной помощью и лечение четырех состояний с невропатической болью: описательное исследование, 2002-2005 гг. BMC Fam Pract . 2008; 9: 26.
3. Лю Л., Ван Х, Лю Н. и др. Остеопороз костей челюсти: фактор, коррелирующий с первичной невралгией тройничного нерва. Медицинский Научный Мониторинг . 2014; 20: 1481-1485.
4. Шапарин Н., Гриценко К., Фернандес Гарсиа-Ровес Д. и др. Периферическая нейромодуляция для лечения рефрактерной невралгии тройничного нерва. Pain Res Manag. 2015; 20 (2): 63-66.
5. Hals EKB, Stubhaug A. Психические и соматические сопутствующие заболевания при хронических состояниях орофациальной боли: пациенты, страдающие болью, нуждаются в многопрофильном командном подходе. Сканд Дж. Боль . 2011; 2 (4): 153-154.
6. Jannetta PJ. Артериальная компрессия тройничного нерва на мосту у пациентов с невралгией тройничного нерва. Дж. Нейросург . 1967; 26 (1 доп.): 159-162.
7. Девор М., Амир Р., Раппапорт Ж. Патофизиология невралгии тройничного нерва: гипотеза воспламенения. Клин Дж. Боль .2002; 18: 4-13.
8. Девор М., Говрин-Липпманн Р., Раппапорт Ж. Механизм невралгии тройничного нерва: ультраструктурный анализ образцов корешка тройничного нерва, полученных во время операции по микрососудистой декомпрессии. Дж. Нейросург . 2002; 96: 532-543.
9. Cruccu G, Finnerup NB, Jensen TS, et al. Невралгия тройничного нерва: новая классификация и диагностическая классификация для практики и исследований. Неврология . 2016; 87 (2): 220-228.
10. Gronseth G, Cruccu G, Alksne J, et al. Параметр практики: диагностическая оценка и лечение невралгии тройничного нерва (обзор, основанный на фактах): отчет Подкомитета по стандартам качества Американской академии неврологии и Европейской федерации неврологических обществ. Неврология . 2008; 71: 1183-1190.
11. Кэмпбелл Ф.Г., Грэм Дж. Г., Зилха К.Дж. Клинические испытания карбазепина (тегретола) при невралгии тройничного нерва. J Neurol Neurosurg Psychiatry . 1966; 29: 265-267.
12. Роклифф Б.В., Дэвис Э. Последовательные контролируемые испытания карбамазепина при невралгии тройничного нерва. Арка Нейрол . 1966; 15: 129-136.
13. Киллиан Дж. М., Фромм Г. Х. Карбамазепин в лечении невралгии. Использование побочных эффектов. Арка Нейрол . 1968; 19: 129-136.
14. Соботка Ю.Л., Александр Б., Повар Б.Л. Обзор гематологических реакций карбамазепина и рекомендации по мониторингу. DICP . 1990; 24 (12): 1214-1219.
15. Минцер С., Боппана П., Тогури Дж. И др. Уровни витамина D и метаболизм костной ткани у пациентов с эпилепсией, принимающих карбамазепин или окскарбазепин . Эпилепсия. 2006; 47 (3): 510-515.
16. Perucca E. Клинически значимые лекарственные взаимодействия с противоэпилептическими препаратами. Br J Clin Pharmacol. , 2006; 61 (3): 246-255.
17.Oomens MA, Forouzanfar T. Фармацевтическое лечение невралгии тройничного нерва у пожилых людей. Препараты старения . 2015; 32 (9): 717-726.
18. Locharernkul C, Shotelersuk V, Hirankarn N. Фармакогенетический скрининг тяжелых кожных аллергических реакций, вызванных карбамазепином. Дж. Clin Neurosci . 2011; 18 (10): 1289-1294.
19. Гулерия В.С., Шарда С., Рана Т., Суд А.К. Вызванный окскарбазепином токсический эпидермальный некролиз — сообщение о редком случае. Индийский J Pharmacol . 2015; 47 (4): 459-461.
20. Линь Л.К., Лай П.С., Ян С.Ф., Ян Р.С. Синдром Стивенса-Джонсона, индуцированный окскарбазепином: клинический случай. Гаосюн Дж. Медицина . 2009; 25 (2): 82-86.
21. Zakrzewska JM, Chaudhry Z, Nurmikko TJ, et al. Ламотриджин (ламиктал) при рефрактерной невралгии тройничного нерва: результаты двойного слепого плацебо-контролируемого перекрестного исследования. Боль . 1997; 73 (2): 223-230.22. Wang XQ, Lv B, Wang HF и др. Тяжелая кожная побочная реакция, вызванная ламотриджином: обновленные данные за 1999-2014 гг. J Clin Neurosci. 2015; 22 (6): 1005-1011.
23. Фромм Г. Х., Терренс К. Ф., Чатта А. С.. Баклофен в лечении невралгии тройничного нерва: двойное слепое исследование и долгосрочное наблюдение. Энн Нейрол . 1984; 15 (3): 240-244.
24. Терренс К.Ф., Фромм Г.Х. Осложнения отмены баклофена. Arch Neurol. 1981; 38 (9): 588-589.
25. Zakrzewska JM. Медикаментозное лечение невропатических болей тройничного нерва. Экспертное мнение Pharmacother . 2010; 11 (8): 1239-1254.
26. Ney JP, Joseph KR.Неврологическое использование ботулинического нейротоксина типа А. Neuropsychiatr Dis Treat . 2007; 3 (6): 785-798.
27. Аврора С.К., Додик Д.В., Тюркель С.К. и др. OnabotulinumtoxinA для лечения хронической мигрени: результаты двойной слепой рандомизированной плацебо-контролируемой фазы исследования PREEMPT 1. Цефалгия . 2010; 30 (7): 793-803.
28. Динер Х.С., Додик Д.В., Аврора С.К. и др. OnabotulinumtoxinA для лечения хронической мигрени: результаты двойной слепой рандомизированной плацебо-контролируемой фазы исследования PREEMPT 2. Цефалгия . 2010; 30 (7): 804-814.
29. Wu C, Xie N, Lian Y, et al. Центральная антиноцицептивная активность периферически применяемого ботулотоксина типа А на модели невралгии тройничного нерва у лабораторных крыс. Springerplus . 2016; 5: 431.
30. Wu CJ, Lian YJ, Zheng YK, et al. Ботулинический токсин типа А для лечения невралгии тройничного нерва: результаты рандомизированного двойного слепого плацебо-контролируемого исследования. Цефалгия . 2012; 32 (6): 443-450.
31. Zhang H, Lian Y, Ma Y, et al.Две дозы ботулотоксина типа А для лечения невралгии тройничного нерва: наблюдение терапевтического эффекта в рандомизированном двойном слепом плацебо-контролируемом исследовании. Дж. Головная боль . 2014; 15:65.
32. Шехата Х.С., Эль-Тамави М.С., Шалаби Н.М., Рамзи Г. Ботулинический токсин типа А: может ли он быть эффективным вариантом лечения трудноизлечимой невралгии тройничного нерва? Дж. Головная боль . 2013; 14: 92.
33. Мендлик М.Т., Урицкий Т.Ю. Лечение невропатической боли. Варианты лечения Curr Neurol .2015; 17 (12): 50.
34. Lechin F, van der Dijs B, Lechin ME, et al. Терапия пимозидом при невралгии тройничного нерва. Арка Нейрол . 1989; 46 (9): 960-963.
35. Чаудри П., Фридман Д.И. Внутривенное лечение лидокаином при классической невралгии тройничного нерва с сопутствующей стойкой лицевой болью. Головная боль . 2014; 54 (8): 1376-1379.
36. Чеширский WP. Фосфенитоин: внутривенное средство для лечения острого криза невралгии тройничного нерва. J Устранение болевых симптомов .2001; 21 (6): 506-510.
37. Bajwa Z, Ho CC, Khan SA. Невралгия тройничного нерва. Дата обновления . www.uptodate.com/contents/trigeminal-neuralgia. По состоянию на 24 августа 2016 г.
Чтобы прокомментировать эту статью, обращайтесь по адресу [email protected].
Более пристальный взгляд на эту загадочную и изнурительную болезнь
Во второй части этой серии из двух частей обсуждается фармацевтическое и хирургическое лечение невралгии тройничного нерва.
Невралгия тройничного нерва (TN), также известная как tic douloureux, является относительно распространенным невропатическим заболеванием, которое характеризуется внезапными сильными приступами стреляющей боли или боли от электрического тока вдоль V черепного нерва (CNV).При ежегодной заболеваемости примерно 4,5 на 100 000 человек TN остается одной из наиболее частых причин лицевых болей во всем мире. 1 В первой части нашей серии из двух частей обсуждались этиология и дифференциальный диагноз TN. 2 В этом выпуске будут рассмотрены фармацевтические и хирургические варианты обезболивания, которые могут помочь уменьшить страдания от этого состояния.
Вы можете прочитать первую часть этой серии статей в выпуске за сентябрь 2012 года.
Фармакотерапия
При выборе правильного лечения пациента с TN врач должен учитывать различные клинические факторы.Международное общество головной боли разделило TN на две категории: классические и вторичные. Хотя обе категории имеют схожие симптомы, они различаются по причинно-следственной связи. Классическая TN включает невралгию, которая является идиопатической или вызвана сдавлением тройничного нерва соседним кровеносным сосудом. Вторичный TN, с другой стороны, объясняет случаи, вызванные другими структурными аномалиями.
В первую очередь необходимо установить, является ли TN идиопатическим / сосудистым или вторичным по происхождению, поскольку большинство вторичных причин, таких как опухоли, не поддаются медикаментозной терапии.Дополнительное внимание также следует уделять клинической картине пациента. Оценивая тяжесть боли, которую испытывает пациент, врач может точно определить, насколько агрессивным должен быть план лечения.
Было доказано, что несколько противоэпилептических препаратов чрезвычайно эффективны при лечении TN. Однако точный механизм, с помощью которого эти препараты приносят пользу пациентам с TN, неизвестен. Более того, нередки случаи, когда пациенты не улучшают состояние после приема лекарств первого ряда.Существует множество препаратов второго ряда, которые доказали свою эффективность; тем не менее, существует ограниченное количество исследований, в которых прямо описывается их эффективность. Опиоиды также играют ограниченную роль в краткосрочном лечении TN, но они требуют высоких доз для достижения адекватного контроля боли. В таблице 1 указаны наиболее распространенные лекарства, назначаемые для лечения TN, их место в иерархии лечения и наиболее заметные побочные эффекты, связанные с ними.
Карбамазепин и окскарбазепин
Благодаря анализу нескольких клинических испытаний карбамазепин стал золотым стандартом лечения TN.Механизм действия карбамазепина, который в основном используется в качестве противоэпилептического средства широкого спектра действия, заключается в подавлении чувствительных к напряжению натриевых каналов, что приводит к заметному снижению потенциалов действия нейронов. Карбамазепин также эффективен в качестве подъемника настроения, что делает этот препарат особенно полезным для пациентов с TN, у которых развиваются симптомы депрессии. После анализа нескольких рандомизированных контролируемых исследований Gronseth et al. Определили, что карбамазепин обеспечивает удовлетворительный контроль боли более чем у 60% пациентов с диагнозом TN. 3 Однако эти многообещающие результаты следует рассматривать вместе с побочными эффектами, наблюдаемыми при применении этого лекарства. Поскольку карбамазепин метаболизируется цитохромом P450-3A4, он может изменять циркулирующие уровни других лекарств, которые метаболизируются тем же путем. Кроме того, карбамазепин может вызывать вестибулярную токсичность, приводящую к нистагму и атаксии. К другим менее частым побочным эффектам относятся агранулоцитоз и апластическая анемия, что требует постоянного мониторинга общего анализа крови.Женщины, прописавшие это лекарство, должны знать, что с карбамазепином связаны различные врожденные дефекты, от дефектов нервной трубки до врожденных пороков сердца.
Чтобы избежать этих осложнений, был разработан окскарбазепин (Трилептал), кето-аналог карбамазепина. Это лекарство, по-видимому, обеспечивает аналогичный уровень контроля боли при лечении TN с менее тревожным профилем побочных эффектов. 3 Хотя лекарственные взаимодействия и вестибулярная токсичность встречаются реже, пациенты, принимающие окскарбазепин, склонны к развитию гипонатриемии.Кроме того, пациенты с определенной генетической предрасположенностью подвержены риску развития синдрома Стивенса-Джонсона при приеме карбамазепина или окскарбазепина.
Пимозид и токаинид
Пимозид (Орап), входящий в группу фенилбутилпиперидина сильнодействующих нейролептиков, в основном используется для лечения синдрома Туретта. Однако в 1989 г. было проведено двойное слепое перекрестное исследование 48 пациентов с ТН, в котором пимозид сравнивался с карбамазепином. В заключение, пимозид обеспечил контроль боли у всех 48 пациентов, в то время как карбамазепин достиг только 56% успеха, что позволяет предположить, что пимозид может быть более эффективным, чем карбамазепин при лечении TN. 4 Несмотря на обнадеживающие результаты, использования пимозида удалось избежать из-за экстрапирамидных побочных эффектов, вызванных его свойствами как антагониста дофамина.
Токинид (Тонокард) — еще одно лекарство, которое было предложено для облегчения боли наравне с карбамазепином. Действуя как антиаритмическое средство класса IB, токаинид вызывает легкую блокировку натриевых каналов, аналогично лидокаину (также класс IB). Использование токаинида при TN затруднено, прежде всего, из-за отсутствия клинических испытаний, демонстрирующих его эффективность.
Баклофен и леветирацетам
При столкновении с пациентами, которые испытывают боль, резистентную к карбамазепину, было предложено использовать большое количество лекарств, хотя клинические доказательства их эффективности не были убедительными. Баклофен представляет собой аналог ɣ-аминомасляной кислоты (ГАМК), который активирует рецепторы ГАМК, что приводит к спазмолитическим свойствам. В исследовании с участием 50 пациентов с ТН, резистентным к карбамазепину, Фромм и др. Пришли к выводу, что при добавлении баклофена к схемам лечения пациентов 74% достигли снижения частоты болезненных эпизодов.Эти результаты были согласованы после периода наблюдения от 1 до 5 лет. 5
Альтернативным лекарством, которое, как сообщалось, было полезно для снижения количества ежедневных приступов рефрактерного TN, является леветирацетам (Keppra). 6 Действуя через неизвестный механизм, леветирацетам, противоэпилептик широкого спектра действия, оказался полезным не только при лечении TN, но и при биполярном расстройстве, а также для профилактики мигрени.
Ламотриджин
Ламотриджин (ламиктал) — еще один вариант лечения рефрактерных случаев TN.Ламотриджин отличается наличием множества механизмов действия, включая ингибирование потенциал-управляемых натриевых и кальциевых каналов, для предотвращения парциальных припадков и припадков синдрома Леннокса-Гасто. В двойном слепом плацебо-контролируемом перекрестном исследовании с 14 пациентами с рефрактерной TN у 11 пациентов (79%) наблюдалось улучшение контроля боли при приеме ламотриджина по сравнению с плацебо. 7 Ламотриджин, как и карбамазепин, связан с синдромом Стивенса-Джонсона и токсическим эпидермальным некролизом; однако этот риск можно уменьшить путем медленного титрования препарата.
Фосфенитоин
Учитывая внезапное начало боли, лекарства, обеспечивающие быстрое облегчение болезненных кризов, оказались необходимыми при лечении TN. Одним из наиболее известных лекарств, удовлетворяющих эту потребность, является фосфенитоин, водорастворимое пролекарство фенитоина. Подобно карбамазепину, фенитоин проявляет свои противоэпилептические эффекты, продлевая рефрактерный период чувствительных к напряжению натриевых каналов. Хорошо известная своим применением при парциальных и генерализованных тонико-клонических припадках, непостоянная биодоступность фенитоина при внутривенном введении приводит к развитию фосфенитоина.Было обнаружено, что при введении во время болевого криза TN внутривенный fosphenytoin обеспечивает безболезненный интервал в 2 дня, чтобы другие лекарства длительного действия подействовали. 8 Хотя обычно используется в острых случаях, врачи должны знать, что фосфенитоин связан с такими же побочными эффектами, как и фенитоин, включая вестибулярную токсичность и сердечно-сосудистую нестабильность.
Другие варианты для пациентов, которым требуется острое облегчение боли в условиях TN, включают инъекции онаботулинического токсина А (ботокс) и суматриптана (имитрекс), хотя последний не следует применять пациентам с ишемической болезнью сердца или тем, кто склонен к эпизодам гипертонии.Лидокаин при интраназальном введении может также обеспечить временное облегчение боли на несколько часов для тех, кто страдает приступом боли. 9
Габапентин и мизопростол
TN классифицируется как классическое или вторичное по отношению к другим системным заболеваниям, таким как рассеянный склероз. Было показано, что некоторые лекарства особенно эффективны, когда TN является вторичным по отношению к рассеянному склерозу, из которых наиболее заметным является габапентин. 10 Габапентин изначально был разработан как агонист рецептора ГАМК; однако было обнаружено, что он действует в первую очередь на пресинаптические кальциевые каналы нейронов, подавляя высвобождение возбуждающих нейротрансмиттеров.Другой предполагаемый механизм его эффекта модуляции боли заключается в его взаимодействии с веществом P, нейропептидом, участвующим в ноцицепции. Габапентин также отличается благоприятным профилем побочных эффектов, наиболее заметными из которых являются умеренный седативный эффект и периферические отеки.
Мизопростол (Cytotec), аналог простагландина E1, также продемонстрировал облегчение симптомов TN, вторичных по отношению к рассеянному склерозу. Обычно используемый для профилактики язв желудка, вызванных нестероидными противовоспалительными препаратами, и в качестве стимулятора матки, исследователи из Чикагского университета вводили мизопростол 7 пациентам с рефрактерным TN, вторичным по отношению к рассеянному склерозу.Из 7 пациентов 6 (86%) сообщили о хотя бы частичном облегчении симптомов. 11
Клоназепам
Клинические испытания, изучающие использование бензодиазепинов при TN, были немногочисленными, что ограничивало эти препараты терапией второй линии. Из этого класса препаратов внимание привлек только клоназепам, бензодиазепин длительного действия. Воздействуя на рецепторы ГАМК, клоназепам увеличивает частоту открытия каналов, что снижает возбудимость нейронов. В исследовании с участием 25 пациентов с TN, большинство из которых были резистентны к карбамазепину, клоназепам смог обеспечить полный контроль боли у 40% пациентов, в то время как еще 23% сообщили о некотором облегчении боли. 12 Эти результаты были омрачены наличием сонливости, которую испытывали более 80% пациентов.
Хирургические вмешательства
Возможности хирургического вмешательства для пациентов с ТН расширились по мере того, как мы стали лучше понимать это заболевание. Пациенты, у которых лицевая боль не поддается адекватной медикаментозной терапии, могут рассмотреть несколько хирургических альтернатив, которые различаются по степени инвазивности и побочных эффектов. Три основных хирургических метода лечения включают: микрососудистую декомпрессию, ризотомию и радиохирургию с использованием гамма-ножа.Консультируя пациентов с рефрактерной TN, клиницисты должны помнить, что эффективность этих хирургических методов лечения зависит не только от конкретного подтипа TN, но и от других сопутствующих заболеваний пациента. Подобно медицинскому лечению, эти хирургические методы по большей части не изучались в крупномасштабных контролируемых испытаниях, детализирующих их степень успеха и частоту рецидивов. Однако было проведено несколько небольших хорошо спланированных клинических испытаний, которые позволяют пациентам иметь разумную оценку рисков и преимуществ каждого хирургического вмешательства.
Микроваскулярная декомпрессия
Поскольку нервно-сосудистая компрессия является наиболее частой причиной TN, неудивительно, что микрососудистая декомпрессия (MVD) является наиболее популярной хирургической терапией, используемой в случаях рефрактерности TN к медикаментозному лечению. Хотя этот метод обычно применяется для классической формы, пациенты с TN, вторичным по отношению к рассеянному склерозу, также могут испытывать некоторое облегчение боли. Перед выполнением МВД хирурги часто проводят ангиографию с магнитно-резонансной томографией (МРТ), чтобы лучше определить взаимосвязь между CNV и сдавливающим сосудом.Тройничный нерв состоит из трех отделов, которые иннервируют различные области лица: глазного нерва (V1), верхнечелюстного нерва (V2) и нижнечелюстного нерва (V3) (рис. 1).
Операция заключается в том, что хирург получает доступ к нервно-сосудистой сети посредством субокципитальной трепанации черепа. После идентификации и выделения CNV и поражающего сосуда, обычно верхней мозжечковой артерии, между нервом и артерией помещают небольшую губку или подушечку, чтобы предотвратить дальнейшую демиелинизацию и раздражение тройничного нерва.Операция завершается очисткой раны физиологическим раствором и заменой отсутствующей затылочной кости небольшой титановой пластиной.
Хотя первоначальные показатели успеха после МВД достигли 90%, частота рецидивов также постепенно увеличивается. Чтобы оценить долгосрочную эффективность МВД, Баркер и др. Наблюдали за 1155 пациентами, перенесшими эту процедуру в течение 20-летнего периода. 13 Спустя 10 лет примерно у 70% пациентов симптомы не проявлялись.Из 30% рецидивов подавляющее большинство произошло в течение 2 лет после операции. Наиболее заметным показателем рецидива было наличие боли вначале после операции. К другим факторам риска относятся принадлежность к женщине и длительность симптомов до операции (> 8 лет) .13 Хотя эти результаты являются многообещающими, процедура сопряжена с определенными рисками. При уровне смертности> 0,5% с МВД связаны многочисленные другие осложнения, включая потерю слуха, паралич экстраокулярных мышц и самоограничивающийся менингизм. 13 Другие менее распространенные побочные эффекты включают инсульт, судороги, утечку спинномозговой жидкости и двоение в глазах.
Ризотомия
Чтобы избежать инвазивности МВД, врачи, лечащие пациентов с рефрактерной ТН, должны рассматривать ризотомию как хирургическую альтернативу. Ризотомия относится к разрушению или перерыву нервов, которые функционируют неправильно. Обычно инициируемая чрескожным доступом, ризотомия прерывает передачу сигналов гиперактивных нервов несколькими методами, включая термокоагуляцию, сжатие баллона и инъекцию химикатов.При достижении немедленного успеха, сопоставимого с МВД, ризотомия связана с более высокой частотой рецидивов и другим набором побочных эффектов. Когда используется термокоагуляция, игла вводится через лицо пациента, когда он находится под частичной анестезией, и располагается рядом с ганглием тройничного нерва. Электрод следует за иглой и использует тепловую энергию для выборочного повреждения тройничного нерва под руководством пациента, который сообщает хирургу, когда его / ее боль уменьшается.Ризотомия с компрессионным баллоном выполняется аналогичным образом, за исключением того, что тройничный нерв повреждается из-за механического сжатия расширяющимся баллоном. Точно так же при химической ризотомии используется глицерин, чтобы прервать передачу боли от тройничного нерва. В раннем послеоперационном периоде эти методы могут облегчить боль> 95% пациентов; однако для длительной ремиссии обычно требуется несколько операций. Более того, каждый метод сопровождается различными побочными эффектами, включая потерю чувствительности лица, менингит и слабость жевательных мышц. 14 Кератит может также возникнуть из-за потери чувствительности роговицы, хотя этот риск минимален при ризотомии с баллонной компрессией. 15 Самым характерным и страшным осложнением ризотомии является анестезия dolorosa, которая характеризуется неослабевающей жгучей болью в лице после операции и не поддается лечению. Помимо жжения, пациенты могут испытывать стреляющую лицевую боль, аналогичную боли при TN. 14
Гамма-нож Радиохирургия
В последние годы использование стереотаксической радиохирургии предоставило еще один неинвазивный хирургический вариант для борьбы с TN.После стабилизации пациента с помощью каркаса головы и проведения местной анестезии установка гамма-ножа может излучать излучение с использованием источников кобальта-60. Затем излучение может напрямую нацеливаться на тройничный нерв. 16 Безопасность этой процедуры зависит от точной доставки гамма-излучения к тройничному нерву, распределение которого обычно отображается до операции с помощью МРТ. Механизм, с помощью которого радиохирургия подавляет передачу боли, не совсем понятен; однако считается, что нарушение эпоптической передачи играет определенную роль. 16
Чтобы определить симптоматическую реакцию на это хирургическое вмешательство, Янг и др. Наблюдали за 60 пациентами с ТН (9 случаев из которых были связаны с опухолью), перенесших стереотаксическую радиохирургию. 17 Из 51 пациента без опухолей 38 пациентов (75%) не испытали боли в течение 4 месяцев после операции. Точно так же из 9 пациентов с опухолями 8 пациентов (89%) сообщили о некотором облегчении боли. 17 Хотя это исследование продемонстрировало немедленные эффекты радиохирургии, средний период наблюдения составил всего 16 месяцев, что оставляет сомнение в его долгосрочной эффективности.
Более продолжительное исследование было проведено Sheehan и соавторами, которые наблюдали за 151 пациентом, получавшим лечение с помощью радиохирургии гамма-ножом в течение 3 лет. Хотя более 90% исследуемых пациентов первоначально испытали некоторое облегчение боли, 27% сообщили о рецидиве боли примерно через 1 год. 18 Эти результаты демонстрируют, что, хотя радиохирургия благоприятна из-за отсутствия осложнений, ее долгосрочная эффективность бледнеет по сравнению с МВД.
Резюме
Тяжесть боли, связанной с TN, и ее разрушительные психологические последствия делают незамедлительную диагностику и лечение очень важными.Без надлежащего понимания клинических особенностей и медицинского течения TN может оставаться невыявленным в течение многих лет, создавая неприемлемое качество жизни для пациентов. После установления диагноза клиницисты должны определить, является ли причина TN вторичной или идиопатической, поскольку схемы лечения различаются в зависимости от основной этиологии. При правильной диагностике и раннем лечении пациенты с этим невропатическим расстройством могут избавиться от боли в течение нескольких недель и вернуться к здоровой и продуктивной жизни.
Последнее обновление: 5 ноября 2012 г.
Не работает лекарство от невралгии тройничного нерва? Узнайте, что делать дальше
Невралгия тройничного нерва сводится к одному: боли. Вот почему это может быть сложно, когда лекарство от невралгии тройничного нерва не работает. Однако существуют и другие варианты лечения, и хотя обычно врач рекомендует в первую очередь медикаментозное лечение, некоторым пациентам для облегчения потребуются другие вмешательства.
Хотя разговор с врачом необходим, может быть полезно получить более полное представление о вашем состоянии, почему лекарства от невралгии тройничного нерва не работают и какие другие варианты лечения могут быть вам доступны.Это расширит ваши возможности в разговоре и поможет вам играть более активную роль в управлении своим состоянием по мере того, как вы переходите к следующему этапу лечения.
О невралгии тройничного нерва
Невралгия тройничного нерва — хроническое болевое заболевание, поражающее области головы и лица. Пациенты, страдающие невралгией тройничного нерва, испытывают повторяющиеся приступы сильной боли, которые могут стать изнурительными, если их не лечить. Основным источником боли является тройничный нерв, который передает ощущения (включая прикосновение и боль) от головы, лица и шеи к мозгу.Однако иногда нерв становится сверхактивным, что приводит к боли без стимуляции.
Невралгией тройничного нерва может быть любой человек, но чаще всего она поражает женщин старше 50 лет. Иногда причина неизвестна, но часто это происходит из-за давления на тройничный нерв, обычно со стороны кровеносного сосуда, которое стимулирует его и вызывает боль. . Это также может быть связано с системными заболеваниями, такими как рассеянный склероз.
Невралгия тройничного нерва до недавнего времени была труднодостижимым заболеванием.Поскольку невозможно сделать убедительные диагностические тесты или изображения, диагноз ставится полностью на основе симптомов пациента, что делает его относительно трудным для диагностики и понимания. Однако благодаря исследованиям и клиническому опыту в области медицины были разработаны новые методы лечения, такие как радиохирургия гамма-ножом.
Почему не действуют ваши лекарства
Существует несколько различных типов лекарств, используемых для лечения невралгии тройничного нерва. Некоторые помогают непосредственно облегчить боль, в то время как другие пытаются облегчить ее, устраняя причину дисфункции.Иногда нерв чрезмерно стимулируется, и лекарства могут помочь предотвратить его чрезмерное возбуждение и причинение боли. В этом случае могут помочь противосудорожные препараты и некоторые антидепрессанты, которые, как правило, являются первым шагом вашего врача при лечении невралгии тройничного нерва.
Однако иногда лекарства от невралгии тройничного нерва не действуют. Это может произойти, потому что ваше состояние является результатом того, что что-то физически давит на нерв и заставляет его срабатывать ненадлежащим образом.Иногда давление вызывает опухоль, но чаще всего причиной является кровеносный сосуд около мозга. В этом случае может потребоваться дальнейшее вмешательство для устранения столкновения с целью облегчения положения.
Ваши следующие шаги
Если вы чувствуете, что лекарство от невралгии тройничного нерва не работает, важно немедленно записаться на прием к врачу. Врач обсудит ваши симптомы и расскажет, получили ли вы какое-либо облегчение от приема лекарств, какие из них и в какой степени.Иногда может потребоваться визуализация, чтобы помочь врачу определить следующие соответствующие шаги. Когда вы переходите к следующему этапу лечения, важно, чтобы вы работали с кем-то, имеющим опыт лечения вашего состояния, например с неврологом.
Гамма-нож при невралгии тройничного нерва
Если ваш врач определит, что структура оказывает давление на тройничный нерв, доступны различные варианты лечения, включая традиционную операцию. Однако существует минимально инвазивный подход, который не требует пребывания в больнице, разрезов и сокращения времени заживления: радиохирургия гамма-ножом.
Несмотря на свое название, Гамма-нож — это не хирургическая процедура, а передовая форма лучевой терапии. Используя несколько высоко сфокусированных лучей излучения, ваш врач может нацелить только на область, подлежащую лечению, щадя здоровые окружающие ткани. В результате пациенты испытывают меньше неприятных побочных эффектов, обычно связанных с лучевой терапией, и их можно лечить за меньшее количество сеансов.
Радиохирургия с использованием гамма-ножавыполняется в амбулаторных условиях, часто в больнице, но не требует пребывания в больнице более двух часов после завершения лечения.Продолжительность сеанса лечения зависит от местоположения и размера обрабатываемой области, но обычно длится от 15 минут до чуть более часа. Многим пациентам требуется всего один сеанс лечения, но это тоже зависит от вашего индивидуального состояния.
Продолжайте искать ответы
Если ваше лекарство от невралгии тройничного нерва не работает, вам не нужно продолжать жить с болью. Существуют и другие варианты лечения, и ваш врач будет работать с вами, чтобы определить следующие шаги в лечении вашего индивидуального состояния.Нет двух абсолютно одинаковых пациентов, и то, что работает для одного человека, не обязательно будет правильным решением для вас.
Самообразование — это фантастический способ сыграть активную роль в вашем здоровье, и узнав как можно больше о своем состоянии и вариантах лечения, вы сможете лучше понять свое состояние. Воспользуйтесь полученной информацией в следующем разговоре со своим врачом и спросите о радиохирургии гамма-ножом для лечения невралгии тройничного нерва.
Невралгия тройничного нерва | Неврология | Mercy Health
Типы невралгии тройничного нерва
Существует два типа невралгии тройничного нерва:
- Тип 1 (TN1) — классическая невралгия тройничного нерва
- Тип 2 (TN2) — атипичная невралгия тройничного нерва
Причины невралгии тройничного нерва
Хотя причина невралгии тройничного нерва до конца не изучена, обычно невралгия тройничного нерва возникает, когда тройничный нерв в основании мозга сдавливается или раздражается кровеносным сосудом.
Причинами давления и последующего износа защитного покрытия нерва могут быть:
- Наличие опухоли головного мозга
- Рассеянный склероз
- Артериовенозная мальформация
- Травма тройничного нерва
Различные движения, влияющие на лицо, могут вызвать приступ, например нанесение макияжа, чистка зубов, умывание, поцелуи, питье, еда или прикосновение к лицу.
Факторы риска невралгии тройничного нерва
- Пол — невралгия тройничного нерва встречается у женщин чаще, чем у мужчин.
- Возраст — по мере старения вы чаще страдаете невралгией тройничного нерва.
- Высокое кровяное давление (гипертония) — у пациентов с высоким кровяным давлением чаще развивается невралгия тройничного нерва.
- Семейный анамнез — если у вас есть родитель с этим заболеванием, у вас также больше шансов заболеть этим заболеванием.
Симптомы невралгии тройничного нерва
Симптомы невралгии тройничного нерва зависят от вашего типа.
Симптомы типа 1 (TN1)
Симптомы невралгии тройничного нерва типа 1 обычно более серьезны, чем симптомы невралгии тройничного нерва.Лицевая боль, вызванная типом 1, возникает внезапно и становится более интенсивной. Боль ощущается как поражение лица электрическим током и может длиться от нескольких минут до нескольких секунд. Обычно разряды происходят последовательно в течение нескольких часов.
Симптомы типа 2 (TN2)
Симптомы невралгии тройничного нерва 2 типа постоянны и больше похожи на тупость, колющие или ноющие ощущения. Невралгия тройничного нерва 2-го типа обычно менее тяжелая, чем тип 1-го типа.
Некоторые пациенты испытывают невралгию тройничного нерва типа 1 и типа 2 одновременно, что может вызвать мучительную боль.
Диагностика невралгии тройничного нерва
Невралгию тройничного нерва может диагностировать невролог. Ваш врач соберет полную историю болезни, оценит ваши симптомы и проведет полное физическое и неврологическое обследование. Во время неврологического осмотра врач будет касаться вашего лица в разных местах, чтобы определить место боли. Врач также проверит рефлексы, чтобы определить, есть ли у вас сдавленный нерв.
Другие тесты для диагностики невралгии тройничного нерва могут включать:
- МРТ (магнитно-резонансная томография) — с помощью МРТ можно получить подробные изображения мозга и сосудов, чтобы определить, есть ли у вас опухоль, рассеянный склероз или другие состояния, которые могут вызывать ваши симптомы.
- Краткий курс противосудорожных препаратов — если ваш врач подозревает, что у вас TN 1-го типа, он или она может назначить противосудорожные препараты, чтобы оценить вашу реакцию на лекарства.
- Низкие дозы трициклических антидепрессантов — у некоторых пациентов может быть диагностирована невралгия тройничного нерва после приема низких доз трициклических антидепрессантов для определения ответа.
Лечение невралгии тройничного нерва
Лечение невралгии тройничного нерва обычно начинается с медикаментозного лечения, а затем, если пациент не отвечает, может потребоваться хирургическое вмешательство.
Виды лекарств для лечения невралгии тройничного нерва
Некоторых пациентов с невралгией тройничного нерва можно лечить только с помощью лекарств. Лекарства могут включать:
- Противосудорожные — противосудорожные препараты более эффективны при невралгии тройничного нерва типа 1; Карбамазепин — широко используемое противосудорожное средство.
- Трициклические антидепрессанты — эти препараты можно использовать для лечения боли у пациентов типа 1 и типа 2. Эти препараты следует применять с осторожностью и под непосредственным наблюдением врача.
- Спазмолитики — спазмолитики используются для расслабления мышц. Их можно использовать вместе с противосудорожными препаратами.
- Инъекции ботокса — Инъекции ботокса доказали свою эффективность в облегчении боли, связанной с невралгией тройничного нерва, у пациентов, которые не реагируют на лекарства.
Хирургические варианты лечения невралгии тройничного нерва
Микроваскулярная декомпрессия
Во время операции микроваскулярной декомпрессии хирург удаляет или перемещает кровеносные сосуды, которые сжимают нерв и вызывают его нарушение.Если ваш врач не может найти кровеносные сосуды, давящие на нерв, он может перерезать нерв. В большинстве случаев эта процедура может успешно устранить боль, связанную с невралгией тройничного нерва. Ваш врач оценит с вами преимущества и риски, когда он или она обсудит с вами эту процедуру.
Излучение гамма-ножом (стереотаксическая радиохирургия)
Во время процедуры гамма-ножа сфокусированные лучи излучения будут направлены на область тройничного нерва, вызывающую ваши симптомы.Цель процедуры — повредить область нерва, вызывающую боль. Ваши симптомы могут не исчезнуть сразу — облегчение симптомов может занять до месяца.
Ризотомия
Во время процедуры ризотомии нервные волокна разрушаются для устранения боли. Существует три типа процедур ризотомии, включая:
- Инъекция глицерина — во время этой процедуры ваш врач введет стерильный глицерин в мешочек с жидкостью, окружающий тройничный нерв, где он разделяется на три ветви.
- Сжатие баллона — во время сжатия баллона ваш врач вставит катетер с баллоном в тройничный нерв, который проходит через основание черепа. Когда он находится в правильном месте, баллон надувается.
- Радиочастотное термическое поражение — во время процедуры радиочастотного термического поражения ваш врач повредит нервные волокна, используя слабый электрический ток, непосредственно на область тройничного нерва, вызывающую ваши симптомы.
Онемение лица после этой процедуры является обычным явлением.
Может ли это быть новым методом лечения невралгии тройничного нерва?
На этой странице:
Компания Regenexx сделала много новинок в области регенеративной медицины. Теперь это может включать новое лечение невралгии тройничного нерва. Давайте углубимся.
Что такое невралгия тройничного нерва?
Vips_s / Shutterstock
Получите второе мнение о своей МРТ или рентгенографии и избегайте ненужной операцииКаковы симптомы невралгии тройничного нерва?
Невралгия тройничного нерва вызывает приступы сильной стреляющей или колющей боли, которая может ощущаться электрической.Приступы могут быть вызваны жеванием, прикосновением к лицу, разговором или чисткой зубов (1). Боль может длиться от нескольких секунд до нескольких минут, и у некоторых пациентов бывают периоды, когда они не испытывают боли. Некоторые приступы могут длиться намного дольше. Боль также может быть спазматической.
Какие стандартные методы лечения невралгии тройничного нерва?
Прежде чем мы перейдем к рассмотрению возможного нового лечения невралгии тройничного нерва. Традиционные методы лечения делятся на следующие категории (2):
- Лекарства
- Противосудорожные препараты: К ним относятся лекарства, стабилизирующие нервы.Обычно это такие препараты, как карбамазепин (Тегретол, Карбатрол и др.), Окскарбазепин (Трилептал), ламотриджин (Ламиктал), фенитоин (Дилантин, Фенитек), клоназепам (Клонопин) и габапентин (Нейронтин, Гралис и др.).
- Мышечные релаксанты: Сюда входит баклофен (Габлофен, Лиорезал).
- Ботокс: Это лекарство, которое можно вводить в мышцы, которое блокирует нервный вход в мышцы и снимает напряжение, спазм и боль.
- Радиация
- Гамма-нож: В этой процедуре используется тот же аппарат, что и для лечения опухолей.Сфокусированный луч излучения направлен на корень тройничного нерва. Эта процедура повреждает тройничный нерв, чтобы попытаться уменьшить или устранить боль. Побочные эффекты могут включать онемение лица.
- Процедуры под визуальным контролем
- Ризотомия: Это разрушение нерва. Используется несколько типов процедур:
- Инъекция глицерина: Игла направляется в область, где нерв выходит из черепа, и вводится глицерин для разрушения нервных волокон.Обычно это вызывает онемение лица.
- Сжатие баллона: Врач вводит полую иглу в часть тройничного нерва, проходящую через основание черепа. Врач вводит в иглу катетер с баллоном на конце. Затем баллон надувается, чтобы повредить тройничный нерв. Опять же, после этой процедуры лицо часто немеет.
- Радиочастотная абляция (РЧА): Врач направляет зонд (который выглядит как игла) в область тройничного нерва.Затем кончик иглы нагревается и разрушает нерв, и снова лицо часто онемеет.
- Ризотомия: Это разрушение нерва. Используется несколько типов процедур:
- Хирургия
- Микроваскулярная декомпрессия: В этой операции хирург перемещает нерв или удаляет кровеносные сосуды, которые контактируют с корешком тройничного нерва. Хирург должен вырезать отверстие в черепе, чтобы добраться до той области, где выходит черепной нерв. Эта операция сопряжена с некоторыми рисками, включая нарушение слуха, слабость лицевых мышц, онемение или инсульт.
Что такое новое лечение невралгии тройничного нерва?
Проблема всех вышеперечисленных методов лечения заключается в том, что все они разрушают нерв. Можем ли мы лечить нерв, чтобы восстановить поврежденный нерв? Мы делаем это с поврежденными нервами в течение многих лет, точно вводя лечебные факторы роста из тромбоцитов крови пациента вокруг нерва. Вот как это выглядит при использовании ультразвукового контроля срединного нерва запястья:
С помощью этой техники мы вылечили синдром запястного канала и повреждение нерва, вызванное хирургическим вмешательством на различных участках.
Присоединяйтесь к нам на бесплатный вебинар Regenexx.Пример нового лечения невралгии тройничного нерва
У этого пациента была невралгия тройничного нерва, и он ранее перенес РЧА. Сначала она увидела доктора Пасторизу (нашего друга в прошлом году), а затем передала лечение доктору Маркл. Оба они использовали точный ультразвуковой и рентгеновский контроль для введения высоких доз лизата тромбоцитов (факторов роста от PRP). Вот что она написала доктору Маркл:
«PRP для лечения невралгии тройничного нерва» Обновление
Мое второе лечение PRP было 16 июня.На этот раз доктор Маркл ввел PRP непосредственно в место столкновения нерва и кровеносного сосуда, а также вдоль нерва. Когда его спросили, он сказал, что хочет видеть улучшение как минимум на 20 процентов. Я молился, чтобы Бог помог мне квалифицировать это.
(1) Я подождал до 7 июля, чтобы перестать использовать ночью обезболивающий. После первой процедуры у меня было всего несколько дней без боли. Я не совсем понимал, чего ожидать на этот раз. Прошло всего две недели с тех пор, как я перестал пользоваться обезболивающим, но у меня совсем нет боли.НЕТ, нада, застежка-молния, ноль. Единственное ощущение, которое я испытываю, — это небольшое давление на «точку». Я на седьмом небе от счастья!
Я знаю, что еще очень рано, и я понятия не имею, как долго я буду без боли, я благодарен и хвалю Бога. Я уверен, вы понимаете, насколько это важно для людей, страдающих невралгией тройничного нерва.
(2) Возникла вторичная проблема. Я сказал об этом доктору Пасторице на нашей первой встрече. Первой моей процедурой была радиохирургия, когда нерв был поврежден, чтобы блокировать болевые сигналы.Боль исчезла, но вся левая половина моей головы онемела от макушки до левого уха и до подбородка. Неплохой компромисс, чтобы избавиться от боли.
Мне сказали, что это может длиться от одного до трех лет. Конечно, я надеялся на три года. В 13 месяцев мое лицо все еще очень онемело. Я бы сказал, что вернулось около 10 процентов чувств. Я думал, когда боль вернется, она вернется медленно, но она вернулась, как товарный поезд, сквозь онемение.
Я хочу сказать, что с тех пор, как я прошел две процедуры PRP, онемение значительно уменьшилось. Онемение ограничивается областью, близкой к месту на пораженном нерве TN, и распространяется прямо по моему лицу к моей левой губе. Я бы сказал, что онемение уменьшилось на 75 процентов. Это большое улучшение! Я ожидаю, что при дальнейшем лечении PRP ситуация будет улучшаться ».
Результат? Это новое лечение невралгии тройничного нерва? Нам придется подождать от нескольких месяцев до года, но если мы сможем спасти этого пациента от большой нейрохирургии, это будет большой победой! Если это сработает, то мы сможем помочь многим пациентам с невралгией тройничного нерва избежать разрушения нервов.
__________________________________________________
Ссылки
(1) Weiss, A.L., Ehrhardt, K.P. И Толба Р. Атипичная лицевая боль: всесторонний, основанный на фактах обзор. Curr Pain Headache Rep 21 , 8 (2017). DOI: 10.1007 / s11916-017-0609-9
(2) Manzoni GC, Torelli P. Эпидемиология типичных и атипичных черепно-лицевых невралгий. Neurol Sci . 2005 May; 26 Suppl 2: s65-7. doi: 10.1007 / s10072-005-0410-0
Chris Centeno, MD , специалист в области регенеративной медицины и новой области интервенционной ортопедии.Centeno была пионером в области ортопедических процедур с использованием стволовых клеток в 2005 году и отвечает за большое количество опубликованных исследований по использованию стволовых клеток в ортопедии. Просмотр профиляЕсли у вас есть вопросы или комментарии по поводу этого сообщения в блоге, напишите нам по адресу [адрес электронной почты защищен]
ПРИМЕЧАНИЕ. В этом сообщении в блоге представлена общая информация, которая поможет читателю лучше понять регенеративную медицину, здоровье опорно-двигательного аппарата и связанные с этим темы.
 , покр. пленочной оболочкой, 200 мг+100 мг+0.2 мг: 10, 20 или 60 шт.
, покр. пленочной оболочкой, 200 мг+100 мг+0.2 мг: 10, 20 или 60 шт.:max_bytes(150000):strip_icc()/trigeminal-neuralgia-and-multiple-sclerosis-2440818_v2-012-b53eaece54614136a4b07402e640acd9.png) 5 или 10 шт.
5 или 10 шт. 100 мг: 10 или 20 шт.
100 мг: 10 или 20 шт. 117 мг: 10 или 20 шт.
117 мг: 10 или 20 шт. пролонгир. действия, покр. пленочной оболочкой, 200 мг: 30 шт.
пролонгир. действия, покр. пленочной оболочкой, 200 мг: 30 шт.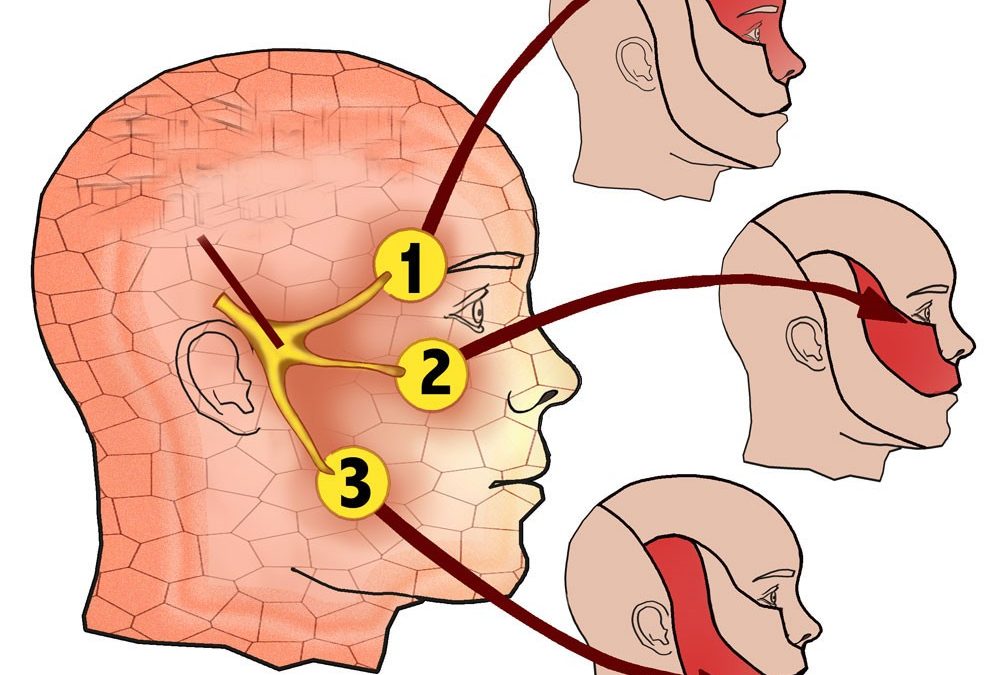
 200 мг: 20, 30 или 50 шт.
200 мг: 20, 30 или 50 шт. 200 мг: 40 или 50 шт.
200 мг: 40 или 50 шт. 200 мг: 10, 20, 30, 40 или 50 шт.
200 мг: 10, 20, 30, 40 или 50 шт. пролонгир. действия 400 мг: 10, 20, 30, 50 или 100 шт.
пролонгир. действия 400 мг: 10, 20, 30, 50 или 100 шт. 200 мг: 20, 30, 50 или 100 шт.
200 мг: 20, 30, 50 или 100 шт. 2 мл 5 или 10 шт.
2 мл 5 или 10 шт. , покр. оболочкой, 100 мг+100 мг: 15, 30 или 60 шт.
, покр. оболочкой, 100 мг+100 мг: 15, 30 или 60 шт. 100 мг: 50 шт.
100 мг: 50 шт. 200 мг: 50 или 100 шт.
200 мг: 50 или 100 шт.